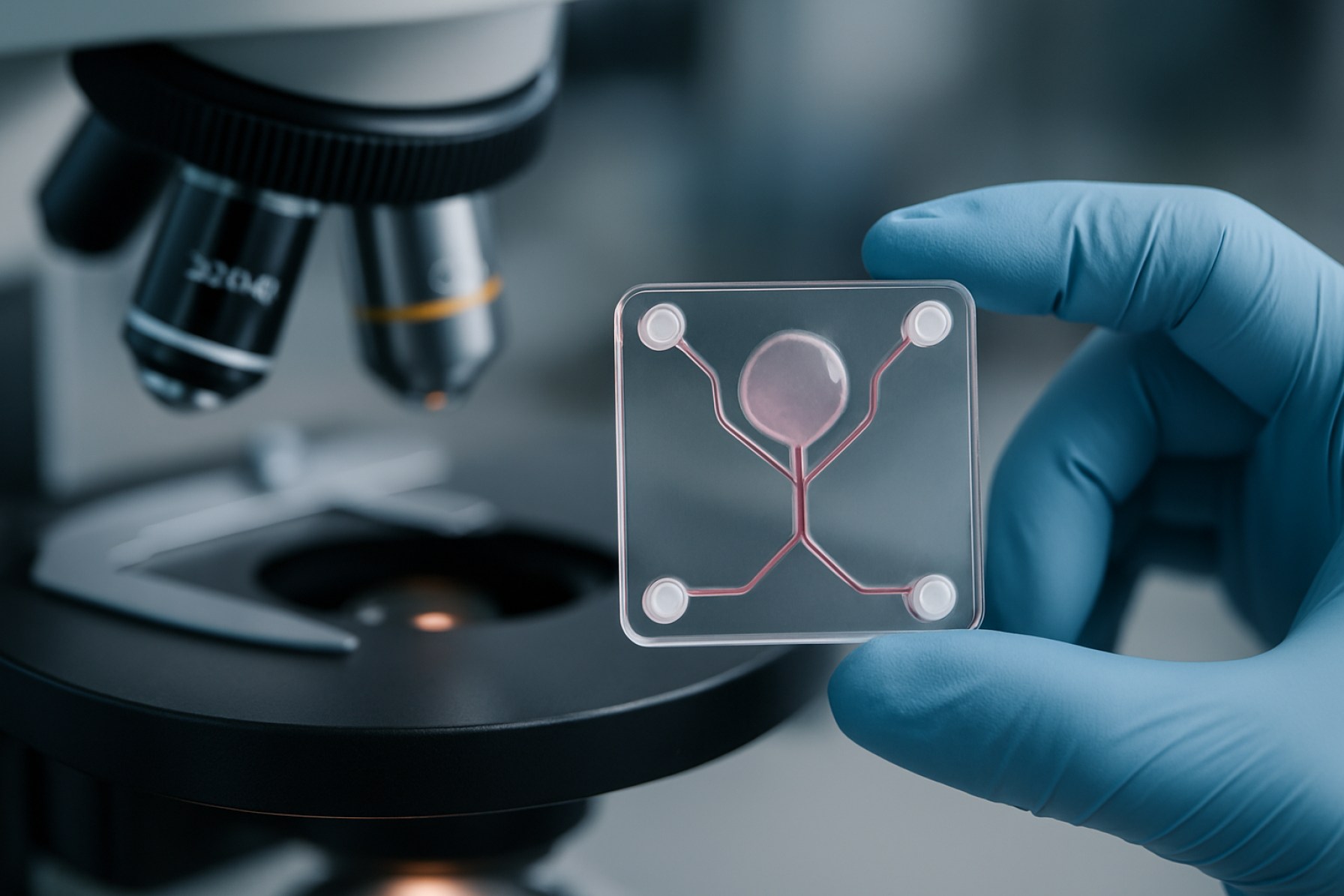
Revolutionierung der biomedizinischen Forschung: Die Prognose für die Mikrofuidik Organ-on-a-Chip-Fertigung im Jahr 2025. Entdecken Sie Marktbeschleunigung, technologische Innovationen und die Zukunft der präzisen Medizin.
- Zusammenfassung: Wichtige Ergebnisse und Marktübersichten
- Marktübersicht: Definition der Mikrofuidik Organ-on-a-Chip-Fertigung im Jahr 2025
- Marktgröße und Prognose (2025–2030): CAGR, Umsatzprognosen und Wachstumsfaktoren
- Wettbewerbslandschaft: Führende Unternehmen, Startups und strategische Allianzen
- Technologische Innovationen: Materialien, Mikrofabricationstechniken und Integrationsfortschritte
- Anwendungen: Wirkstoffforschung, Toxikologie, Krankheitsmodellierung und personalisierte Medizin
- Regulatorisches Umfeld und Standardisierungsbemühungen
- Regionale Analyse: Nordamerika, Europa, Asien-Pazifik und aufstrebende Märkte
- Herausforderungen und Barrieren: Skalierbarkeit, Kosten und Adoptierungsbarrieren
- Zukünftige Aussichten: Disruptive Trends, Investitionshotspots und Marktchancen
- Anhang: Methodik, Datenquellen und Marktwachstumsprognose (geschätzte CAGR: 18–22 % 2025–2030)
- Quellen & Referenzen
Zusammenfassung: Wichtige Ergebnisse und Marktübersichten
Der Markt für die Mikrofuidik Organ-on-a-Chip (OoC) Fertigung steht im Jahr 2025 vor erheblichem Wachstum, angetrieben von Fortschritten in der Mikroengineering, Biomaterialien und der zunehmenden Nachfrage nach physiologisch relevanten in vitro Modellen. Organ-on-a-Chip-Geräte, die lebende Zellen innerhalb von Mikrofuidiksystemen integrieren, um die Funktionen auf Organeebene zu simulieren, revolutionieren die Wirkstoffforschung, Toxikologietests und die Krankheitsmodellierung. Der Markt verzeichnet robuste Investitionen aus dem öffentlichen und privaten Sektor, wobei wichtige Akteure wie Emulate, Inc., MIMETAS B.V. und CN Bio Innovations Ltd. führend in Innovation und Kommerzialisierung sind.
Zentrale Ergebnisse zeigen, dass die Einführung von Mikrofuidik OoC-Plattformen in der pharmazeutischen und biotechnologischen Industrie beschleunigt wird, hauptsächlich aufgrund ihrer Fähigkeit, vorhersehbarere, menschenrelevante Daten im Vergleich zu traditionellen Zellkultur- und Tiermodellen bereitzustellen. Regulierungsbehörden, einschließlich der U.S. Food and Drug Administration (FDA), erkennen zunehmend das Potenzial von OoC-Technologien, um präklinische Tests zu verbessern, und treiben damit das Marktwachstum weiter voran.
Technologische Fortschritte in der Mikrofabrication—wie 3D-Druck, Softlithografie und fortschrittliche Polymermaterialien—ermöglichen die Herstellung komplexerer und skalierbarer Chip-Designs. Dies fördert die Entwicklung von Multi-Organ-Chips und Plattformen für Hochdurchsatz-Screening, was den Anwendungsbereich von Einzelorganmodellen auf integrierte Mensch-auf-einem-Chip-Systeme erweitert. Zusammenarbeit zwischen akademischen Institutionen, Branchenführern und Regulierungsbehörden fördert Standardisierungs- und Validierungsbemühungen, die für eine breitere Akzeptanz entscheidend sind.
Geografisch bleiben Nordamerika und Europa an der Spitze der Marktaktivitäten, unterstützt durch eine starke Forschungsinfrastruktur und Finanzierungsinitiativen. Asien-Pazifik entwickelt sich jedoch zu einer wachstumsstarken Region, mit zunehmenden Investitionen in biomedizinische Forschung und einer wachsenden Präsenz lokaler Hersteller.
Zusammenfassend lässt sich sagen, dass der Markt für die Mikrofuidik Organ-on-a-Chip Fertigung im Jahr 2025 durch schnellen technologischen Fortschritt, erweiterte Anwendungsbereiche und zunehmende regulatorische Akzeptanz geprägt ist. Diese Trends werden voraussichtlich weiter Investitionen und Innovationen anziehen und OoC-Technologien als Grundpfeiler der biomedizinischen Forschung und Arzneimittelentwicklung der nächsten Generation positionieren.
Marktübersicht: Definition der Mikrofuidik Organ-on-a-Chip-Fertigung im Jahr 2025
Die Mikrofuidik Organ-on-a-Chip-Fertigung repräsentiert einen transformativen Ansatz in der biomedizinischen Technik, der die Rekonstruktion menschlicher Organfunktionen auf mikroskaligen Geräten ermöglicht. Bis 2025 wird diese Technologie voraussichtlich eine zentrale Rolle in der Wirkstoffforschung, Toxikologie und Krankheitsmodellierung spielen und physiologisch relevantere Alternativen zur traditionellen Zellkultur und Tierversuchen bieten. Der Kern der Organ-on-a-Chip-Systeme liegt in ihrer Fähigkeit, lebende Zellen innerhalb von Mikrofuidikkanälen zu integrieren, was die dynamische Mikroumgebung menschlicher Gewebe und Organe simuliert.
Der Markt für die Mikrofuidik Organ-on-a-Chip-Fertigung ist durch schnelle Innovation und zunehmende Akzeptanz in den Bereichen Pharma, Biotechnologie und akademische Forschung geprägt. Die wichtigsten Antriebskräfte sind die Nachfrage nach prädiktiveren präklinischen Modellen, die Notwendigkeit, die Abhängigkeit von Tierversuchen zu verringern, und regulatorische Ermutigung für alternative Testmethoden. Im Jahr 2025 erleben wir die Konvergenz fortschrittlicher Materialien, wie biokompatibler Polymere und Hydrogels, mit präzisen Mikrofabricationstechniken wie Softlithografie und 3D-Druck. Diese Fortschritte ermöglichen die Produktion von Chips, die komplexe Funktionen auf Organeebene nachahmen können, einschließlich Vaskularisation, mechanischer Stimulation und Interaktionen zwischen mehreren Organen.
Führende Organisationen wie Emulate, Inc. und MIMETAS B.V. stehen an der Spitze und bieten kommerzielle Plattformen an, die Hochdurchsatz-Screening und anpassbare Organmodelle unterstützen. Akademische und industrielle Kooperationen beschleunigen weiter die Übersetzung von Organ-on-a-Chip-Technologien aus dem Labor in die praktischen Anwendungen, wobei Regulierungsbehörden wie die U.S. Food and Drug Administration (FDA) aktiv deren Einsatz in der Bewertung von Arzneimittelsicherheit und -wirksamkeit prüfen.
Bis 2025 wird die Marktlandschaft auch durch die Integration von Sensortechnologien und Echtzeitanalysen geprägt, die eine kontinuierliche Überwachung der zellulären Reaktionen und der mikroökologischen Bedingungen ermöglichen. Diese Fähigkeit erhöht den Wert von Organ-on-a-Chip-Systemen für die personalisierte Medizin und präzise Therapien. Mit dem Reifegrad des Bereichs werden Standardisierungsbemühungen, die von Organisationen wie ASTM International geleitet werden, voraussichtlich eine breitere Akzeptanz und Interoperabilität zwischen den Plattformen fördern.
Zusammenfassend lässt sich sagen, dass die Mikrofuidik Organ-on-a-Chip-Fertigung im Jahr 2025 durch technologische Raffinesse, erweiterte kommerzielle Angebote und zunehmende regulatorische Akzeptanz definiert ist, was sie zu einem Grundpfeiler der biomedizinischen Forschung und Entwicklung der nächsten Generation macht.
Marktgröße und Prognose (2025–2030): CAGR, Umsatzprognosen und Wachstumsfaktoren
Der globale Markt für die Mikrofuidik Organ-on-a-Chip-Fertigung steht zwischen 2025 und 2030 vor erheblichem Wachstum, angetrieben von Fortschritten in der biomedizinischen Forschung, Arzneimittelentwicklung und personalisierter Medizin. Laut Branchenanalysen wird erwartet, dass der Markt in diesem Zeitraum eine jährliche Wachstumsrate (CAGR) von etwa 20–25 % erzielen wird, wobei die Umsatzprognosen mehrere Milliarden USD bis 2030 erreichen werden. Dieses robuste Wachstum wird durch die zunehmende Nachfrage nach physiologisch relevanten in vitro Modellen untermauert, die die Funktionen menschlicher Organe genauer nachahmen können als traditionelle Zellkulturen oder Tiermodelle.
Die wichtigsten Wachstumsfaktoren sind die zunehmende Akzeptanz von Organ-on-a-Chip-Plattformen durch pharmazeutische und biotechnologische Unternehmen für präklinisches Screening und Toxikologietests. Diese Mikrofuidikgeräte bieten verbesserte Prädiktionskraft für menschliche Reaktionen, verringern die Abhängigkeit von Tierversuchen und beschleunigen den Arzneimittelentwicklungsprozess. Darüber hinaus erkennen Regulierungsbehörden wie die U.S. Food and Drug Administration zunehmend den Wert von Organ-on-a-Chip-Technologien in der regulatorischen Wissenschaft, was deren Integration in Forschungs- und Entwicklungsabläufe weiter fördert.
Technologische Innovationen in der Mikrofabrication, wie fortgeschrittener 3D-Druck und Softlithografie, treiben das Marktwachstum ebenfalls voran, indem sie die Produktion komplexerer und skalierbarer Organ-on-a-Chip-Systeme ermöglichen. Führende Unternehmen und Forschungseinrichtungen, darunter Emulate, Inc. und CN Bio Innovations, investieren erheblich in Forschung und Entwicklung, um ihre Produktportfolios zu erweitern und die Reproduzierbarkeit und den Durchsatz der Geräte zu verbessern.
Geografisch werden Nordamerika und Europa voraussichtlich dominante Marktanteile behalten, dank einer starken Forschungsinfrastruktur, finanzieller Unterstützung und der Präsenz wichtiger Akteure der Branche. Die Region Asien-Pazifik wird jedoch voraussichtlich das schnellste Wachstum verzeichnen, angetrieben durch zunehmende Investitionen in die Lebenswissenschaften und einen wachsenden Fokus auf innovative Gesundheitslösungen.
Zusammenfassend lässt sich sagen, dass der Markt für die Mikrofuidik Organ-on-a-Chip-Fertigung bis 2030 voraussichtlich schnell wachsen wird, angetrieben durch technologische Fortschritte, regulatorische Unterstützung und den dringenden Bedarf an prädiktiveren und ethischen präklinischen Testmodellen. Während der Bereich reift, werden Kooperationen zwischen Wissenschaft, Industrie und Regulierungsbehörden entscheidend sein, um die Marktlandschaft zu gestalten und die Akzeptanz dieser transformativen Technologien zu beschleunigen.
Wettbewerbslandschaft: Führende Unternehmen, Startups und strategische Allianzen
Die Wettbewerbslandschaft der Mikrofuidik Organ-on-a-Chip (OoC) Fertigung im Jahr 2025 ist geprägt von einem dynamischen Zusammenspiel zwischen etablierten Branchenführern, innovativen Startups und einer wachsenden Anzahl strategischer Allianzen. Dieser Sektor wird durch die Notwendigkeit, physiologisch relevante in vitro Modelle für die Wirkstoffforschung, Toxikologietests und Krankheitsmodellierung zu entwickeln, vorangetrieben, was die Unternehmen dazu drängt, sowohl im Gerätdesign als auch in den Produktionsprozessen innovativ zu sein.
Unter den führenden Akteuren setzt Emulate, Inc. weiterhin Maßstäbe mit seinen kommerzialisierten Organ-on-a-Chip-Plattformen, die eine Reihe von Chips anbieten, die menschliche Organe wie die Lunge, die Leber und den Darm nachahmen. MIMETAS ist ein weiterer wichtiger Akteur, bekannt für seine OrganoPlate®-Plattform, die Mikrofuidik-Technologie für Hochdurchsatz-Screening und 3D-Gewebekultur nutzt. CN Bio Innovations hat sich ebenfalls mit Einzel- und Multi-Organ-Mikrophysiologischen Systemen etabliert, die sich auf Anwendungen in der Arzneimittelmetabolisierung und Toxizität konzentrieren.
Das Startup-Ökosystem ist lebendig, mit Unternehmen wie Tissium und Nortis, die neuartige Fertigungstechniken und spezialisierte Chips für Nischenanwendungen wie vaskularisierte Gewebemodelle und personalisierte Medizin entwickeln. Diese Startups entstehen häufig aus akademischen Spin-offs und nutzen Spitzentechnologien, um spezifische Lücken im Markt zu schließen, wie Skalierbarkeit, Integration mit Biosensoren oder Kompatibilität mit automatisierten Workflows.
Strategische Allianzen prägen zunehmend den Sektor, da Unternehmen versuchen, Fachwissen in Mikrofabrication, Zellbiologie und Datenanalyse zu kombinieren. Zum Beispiel hat Emulate, Inc. mit großen Pharmaunternehmen und Regulierungsbehörden zusammengearbeitet, um seine Plattformen für präklinische Tests zu validieren. In ähnlicher Weise kooperiert MIMETAS mit akademischen Einrichtungen und Industriepartnern, um die Palette der Organmodelle zu erweitern und die Durchsatzkapazitäten zu verbessern.
Insgesamt ist die Wettbewerbslandschaft im Jahr 2025 geprägt von schnellen technologischen Fortschritten, interdisziplinären Kooperationen und einem Fokus auf Standardisierung und regulatorische Akzeptanz. Dieses Umfeld fördert sowohl einen gesunden Wettbewerb als auch synergetische Partnerschaften und beschleunigt die Akzeptanz der Mikrofuidik Organ-on-a-Chip-Technologien in der biomedizinischen Forschung und pharmazeutischen Entwicklung.
Technologische Innovationen: Materialien, Mikrofabricationstechniken und Integrationsfortschritte
In den letzten Jahren hat es bedeutende technologische Innovationen in der Fertigung von Mikrofuidik Organ-on-a-Chip (OoC) Geräten gegeben, die durch die Notwendigkeit für physiologisch relevante in vitro Modelle vorangetrieben werden. Fortschritte in der Materialwissenschaft haben die Palette der Substrate über das traditionelle Polydimethylsiloxan (PDMS) hinaus erweitert, um Probleme wie die Absorption kleiner Moleküle und begrenzte Skalierbarkeit anzugehen. Thermoplastische Materialien wie zyklischer Olefin-Copolymer (COC) und Polymethylmethacrylat (PMMA) werden zunehmend aufgrund ihrer optischen Klarheit, Biokompatibilität und Eignung für die Massenproduktion durch Spritzgießen übernommen. Darüber hinaus werden Hydrogels und bioaktive Polymere entwickelt, um die extrazelluläre Matrix besser nachzuahmen, was komplexere Gewebearchitekturen und dynamische Zellinteraktionen unterstützt.
Die Mikrofabricationstechniken haben sich ebenfalls weiterentwickelt, von konventioneller Softlithografie hin zu vielseitigeren und skalierbaren Methoden. Hochauflösende 3D-Drucktechniken, einschließlich Zwei-Photonen-Polymerisation und digitale Lichtverarbeitung, ermöglichen die schnelle Prototypenerstellung komplexer Mikrokanelnetzwerke und mehrschichtiger Strukturen. Lasermikromaschinen und Heißprägen verbessern die Präzision und den Durchsatz der Geräteproduktion weiter. Diese Techniken ermöglichen die Integration mehrerer Zelltypen, vaskuläre Netzwerke und mechanische Aktuationselemente innerhalb eines einzigen Chips, wodurch die Funktionen auf Organeebene genau nachgeahmt werden.
Integrationsfortschritte sind zentral für die nächste Generation von OoC-Plattformen. Die Integration von embeded Sensors—wie Elektroden für elektrische Ausgaben, optischen Sensoren für Echtzeitbilder und mikrofuidischen Ventilen für dynamische Steuerung des Flusses—ermöglicht die kontinuierliche Überwachung von zellulären Reaktionen und Umweltbedingungen. Modulardesign-Strategien ermöglichen die Verbindung mehrerer Organ-Chips, die multi-organ oder “Körper-auf-einem-Chip” Systeme unterstützen, die systemische Interaktionen besser simulieren. Darüber hinaus fördert die Annahme standardisierter Schnittstellen und Open-Source-Hardware die Interoperabilität und Reproduzierbarkeit zwischen Forschungsgruppen und Industriepartnern.
Diese technologischen Innovationen werden durch kollaborative Bemühungen zwischen akademischen Institutionen, Branchenführern und Regulierungsbehörden vorangetrieben. Zum Beispiel sind Emulate, Inc. und MIMETAS B.V. Pioniere kommerzieller OoC-Plattformen mit fortschrittlichen Material- und Integrationsfunktionen, während Organisationen wie die U.S. Food and Drug Administration (FDA) diese Technologien aktiv auf regulatorische Akzeptanz prüfen. Wenn sich diese Innovationen weiterentwickeln, wird erwartet, dass sie die Akzeptanz von OoC-Systemen in der Arzneimittelentwicklung, Krankheitsmodellierung und personalisierter Medizin beschleunigen.
Anwendungen: Wirkstoffforschung, Toxikologie, Krankheitsmodellierung und personalisierte Medizin
Mikrofuidik Organ-on-a-Chip (OoC) Plattformen haben die Bereiche Wirkstoffforschung, Toxikologie, Krankheitsmodellierung und personalisierte Medizin rasant vorangebracht, indem sie physiologisch relevante in vitro Modelle bereitstellen, die die Funktionen menschlicher Organe nachahmen. Diese mikroin engineered Systeme, die mithilfe von Techniken wie Softlithografie, 3D-Druck und Photolithografie hergestellt werden, ermöglichen eine präzise Kontrolle über zelluläre Mikroumgebungen, Flüssigkeitsfluss und Gewebe-Grenzflächen, die für die Nachahmung der Komplexität menschlicher Organe entscheidend sind.
In der Wirkstoffforschung ermöglichen OoC-Geräte Hochdurchsatz-Screenings von pharmazeutischen Verbindungen unter Bedingungen, die der menschlichen Physiologie nahekommen. Dies verringert die Abhängigkeit von Tiermodellen und traditionellen Zellkulturen, die oft nicht in der Lage sind, menschliche Reaktionen genau vorherzusagen. Beispielsweise wurden Leber-auf-einem-Chip und Herz-auf-einem-Chip Systeme verwendet, um Arzneimittelmetabolismus und Kardiotoxizität zu bewerten und frühe Einblicke in Wirksamkeits- und Sicherheitsprofile zu geben. Unternehmen wie Emulate, Inc. und MIMETAS B.V. haben kommerzielle Plattformen entwickelt, die zunehmend von Pharmaunternehmen für präklinische Tests übernommen werden.
Toxikologiestudien profitieren von der OoC-Technologie, indem sie die Bewertung der Auswirkungen chemischer und umweltbedingter Toxine auf menschliche Gewebe ermöglichen. Modelle wie Lunge-auf-einem-Chip und Niere-auf-einem-Chip waren beispielsweise maßgeblich bei der Bewertung der Auswirkungen von Luftverschmutzung und nephrotoxischen Arzneimitteln. Diese Systeme bieten eine Echtzeitüberwachung zellulärer Reaktionen, der Barriereintegrität und der Gewebeviabilität und bieten somit eine prädiktivere und ethische Alternative zu Tierversuchen. Regulierungsbehörden wie die U.S. Food and Drug Administration erkunden aktiv die Integration von OoC-Daten in Sicherheitsbewertungsprozesse.
Die Krankheitsmodellierung ist eine weitere transformative Anwendung, bei der OoC-Plattformen verwendet werden, um pathologische Bedingungen wie Krebs, neurodegenerative Erkrankungen und Infektionskrankheiten nachzubilden. Durch die Integration von patientenabgeleiteten Zellen können Forscher den Krankheitsverlauf, die Wirts-Pathoogen-Interaktionen und therapeutische Reaktionen in einer kontrollierten Mikroumgebung untersuchen. Dieser Ansatz hat sich besonders als wertvoll erwiesen, um seltene Krankheiten zu modellieren und Mechanismen zu verstehen, die in vivo schwer zu erfassen sind.
Die personalisierte Medizin wird voraussichtlich erheblich von der OoC-Technologie profitieren. Durch die Integration von patientenspezifischen Zellen in Organ-Chips ist es möglich, individuelle Reaktionen auf Arzneimittel vorherzusagen und Behandlungen entsprechend anzupassen. Dieser personalisierte Ansatz wird von Organisationen wie CN Bio Innovations untersucht, die Leber-auf-einem-Chip-Systeme für Anwendungen in der präzisen Medizin entwickeln. Während sich die Fertigungstechniken weiterentwickeln, wird die Skalierbarkeit und Reproduzierbarkeit von OoC-Geräten voraussichtlich ihre Auswirkungen in der biomedizinischen Forschung und klinischen Praxis weiter erhöhen.
Regulatorisches Umfeld und Standardisierungsbemühungen
Das regulatorische Umfeld und die Standardisierungsbemühungen rund um die Mikrofuidik Organ-on-a-Chip (OoC) Fertigung entwickeln sich schnell, während diese Technologien von der akademischen Forschung in kommerzielle und klinische Anwendungen übergehen. Regulierungsbehörden wie die U.S. Food and Drug Administration (FDA) und die European Medicines Agency (EMA) treten zunehmend in Dialog mit Interessengruppen, um Rahmenbedingungen zu entwickeln, die die Sicherheit, Zuverlässigkeit und Reproduzierbarkeit von OoC-Geräten gewährleisten. Diese Behörden erkennen das Potenzial von OoC-Systemen, die Abhängigkeit von Tierversuchen zu verringern und die prädiktive Leistung präklinischer Arzneimittelbewertungen zu verbessern.
Eine Schlüsselherausforderung im regulatorischen Umfeld ist das Fehlen allgemein akzeptierter Standards für das Design, die Fertigung und die Validierung von mikrofuidischen OoC-Plattformen. Um dies anzugehen, haben Organisationen wie ASTM International und die Internationale Organisation für Normung (ISO) Arbeitsgruppen ins Leben gerufen, die sich auf die Entwicklung von Konsensstandards für Materialien, Geräteleistung und biologische Validierung konzentrieren. Diese Bemühungen zielen darauf ab, Testprotokolle, Datenberichterstattung und Qualitätskontrollmaßnahmen zu harmonisieren, um die regulatorische Akzeptanz und die Reproduzierbarkeit zwischen Laboren zu erleichtern.
Im Jahr 2025 beschleunigen kollaborative Initiativen zwischen Industrie, Wissenschaft und Regulierungsbehörden die Festlegung von Best Practices. Beispielsweise unterstützt das National Centre for the Replacement, Refinement and Reduction of Animals in Research (NC3Rs) im Vereinigten Königreich aktiv die Entwicklung von OoC-Validierungsrichtlinien, um sicherzustellen, dass diese Modelle zuverlässig in regulatorischen Einreichungen verwendet werden können. In ähnlicher Weise fördern die National Institutes of Health (NIH) in den Vereinigten Staaten Konsortien, die sich auf die Standardisierung von Fertigungsprozessen und biologischen Endpunkten für OoC-Systeme konzentrieren.
Trotz dieser Fortschritte bestehen weiterhin Schwierigkeiten, die globalen regulatorischen Anforderungen abzustimmen und sicherzustellen, dass die Standards mit den schnellen technologischen Innovationen Schritt halten. Ein ständiger Dialog zwischen Geräteherstellern, Endbenutzern und Regulierungsbehörden ist entscheidend, um Herausforderungen wie Geräteskalierbarkeit, Integration in bestehende Laborabläufe und langfristige Biokompatibilität anzugehen. Wenn die Standardisierungsbemühungen reifen, wird erwartet, dass sie den Weg zur regulatorischen Genehmigung vereinfachen, das industrielle Wachstum fördern und letztendlich die Auswirkungen der Mikrofuidik Organ-on-a-Chip-Technologien in biomedizinischer Forschung und Arzneimittelentwicklung erhöhen.
Regionale Analyse: Nordamerika, Europa, Asien-Pazifik und aufstrebende Märkte
Die globale Landschaft der Mikrofuidik Organ-on-a-Chip-(OoC)-Fertigung ist durch erhebliche regionale Unterschiede in der Forschungsintensität, Kommerzialisierung und regulatorischen Rahmenbedingungen geprägt. In Nordamerika, insbesondere in den Vereinigten Staaten, wird der Sektor durch umfangreiche Mittel von Einrichtungen wie den National Institutes of Health und ein starkes Ökosystem akademischer und industrieller Partnerschaften angetrieben. Führende Universitäten und Startups arbeiten zusammen, um die Komplexität und den Durchsatz der Chips voranzutreiben, mit einem Fokus auf Anwendungen in der Wirkstoffforschung und Toxikologie. Die Präsenz großer Pharmaunternehmen und ein unterstützendes regulatorisches Umfeld beschleunigen zudem die Akzeptanz von OoC-Technologien.
In Europa liegt der Schwerpunkt auf Standardisierung, grenzüberschreitenden Kooperationen und ethischen Überlegungen. Das Horizon-Europa-Programm der Europäischen Union finanziert multinationalen Projekte, die darauf abzielen, die Fertigungsprotokolle zu harmonisieren und OoC-Plattformen in präklinische Testpipeline zu integrieren. Deutschland, die Niederlande und das Vereinigte Königreich beherbergen Innovationscluster, in denen Unternehmen und Forschungsinstitute daran arbeiten, Herausforderungen in Bezug auf Skalierbarkeit und Reproduzierbarkeit zu bewältigen. Regulierungsbehörden in Europa engagieren sich ebenfalls aktiv mit Industrievertretern, um Richtlinien für die Validierung und Akzeptanz von OoC-Daten in regulatorischen Einreichungen zu entwickeln.
Die Region Asien-Pazifik, angeführt von China, Japan und Singapur, erlebt ein rapides Wachstum in der Mikrofuidik OoC-Fertigung. Regierungen investieren stark in Infrastruktur für Biotechnologie, und akademische Institutionen produzieren hochkarätige Forschung zu neuartigen Chipmaterialien und integrierten Sensortechnologien. Die Fertigungskompetenz der Region ermöglicht eine kostengünstige Produktion und schnelle Prototypenentwicklung, was Asien-Pazifik zu einem Schlüsselakteur in der globalen Lieferkette für Mikrofuidikkomponenten macht. Strategische Partnerschaften zwischen lokalen Unternehmen und globalen Pharmafirmen fördern auch den Technologietransfer und die Marktexpansion.
Aufstrebende Märkte in Lateinamerika, dem Mittleren Osten und Afrika treten allmählich in den OoC-Sektor ein, hauptsächlich durch akademische Kooperationen und Pilotprojekte. Obwohl die Infrastruktur und Finanzierung im Vergleich zu etablierten Regionen begrenzt bleiben, helfen Initiativen, die von Organisationen wie der Weltgesundheitsorganisation unterstützt werden, lokale Kapazitäten aufzubauen. Diese Märkte werden voraussichtlich von Technologietransfer und der Anpassung von OoC-Plattformen an regionalspezifische Gesundheitsherausforderungen profitieren, wie z.B. der Modellierung von Infektionskrankheiten und umweltbedingter Toxikologie.
Insgesamt spiegeln die regionalen Dynamiken in der Mikrofuidik Organ-on-a-Chip-Fertigung unterschiedliche Prioritäten wider, von Innovation und Kommerzialisierung in Nordamerika und Asien-Pazifik bis hin zu Standardisierung und ethischer Überwachung in Europa, während aufstrebende Märkte auf eine schrittweise Integration in das globale Ökosystem vorbereitet sind.
Herausforderungen und Barrieren: Skalierbarkeit, Kosten und Adoptierungsbarrieren
Trotz signifikanter Fortschritte in der Mikrofuidik Organ-on-a-Chip (OoC) Technologie stehen mehrere Herausforderungen der breiten Akzeptanz und industriellen Skalierbarkeit entgegen. Eine der Haupthürden ist die Komplexität der Fertigungsprozesse. Die meisten OoC-Geräte werden mithilfe von Softlithografie mit Polydimethylsiloxan (PDMS) produziert, eine Methode, die zwar präzise ist, aber arbeitsintensiv und schwer in die Massenproduktion zu skalieren ist. Der Übergang zu alternativen Materialien und Fertigungstechniken, wie Thermoplasten und Spritzguss, ist im Gange, erfordert jedoch erhebliche Investitionen in neue Infrastruktur und Prozessoptimierung (Dolomite Microfluidics).
Kosten bleiben ein bedeutendes Hindernis. Der hohe Preis für maßgeschneiderte Mikrofabrication, spezialisierte Materialien und der Bedarf an qualifiziertem Personal tragen zu den Gesamtkosten von OoC-Geräten bei. Dies schränkt den Zugang für kleinere Forschungslabore ein und verlangsamt den Innovationsprozess. Darüber hinaus erhöht die Integration mehrerer Zelltypen und die Nachbildung komplexer Gewebeoberflächen auf einem einzelnen Chip sowohl die technische Schwierigkeit als auch die Produktionskosten (Emulate, Inc.).
Die Akzeptanz wird auch durch das Fehlen von Standardisierung in der Branche behindert. Die Variabilität im Geräte-Design, Materialien und Protokollen macht es schwierig, Ergebnisse zwischen Studien zu vergleichen oder OoC-Modelle für regulatorische Zwecke zu validieren. Regulierungsbehörden wie die U.S. Food and Drug Administration arbeiten mit den Stakeholdern der Branche zusammen, um Richtlinien zu entwickeln, doch die Harmonisierung steht noch am Anfang. Zudem erfordert die Integration von OoC-Plattformen in bestehende Arzneimittelentwicklungsprozesse erhebliche Änderungen in Workflow und Datenmanagement, was für etablierte Pharmaunternehmen ein Hemmnis darstellen kann (European Federation of Pharmaceutical Industries and Associations).
Schließlich ist die biologische Komplexität menschlicher Organe schwierig vollständig auf einem Chip nachzubilden. Die Gewährleistung langfristiger Zellviabilität, funktionaler Gewebeoberflächen und physiologisch relevanter Reaktionen bleibt eine technische Herausforderung. Diese Beschränkungen beeinträchtigen die prädiktive Leistung von OoC-Modellen und deren Akzeptanz als Alternativen zu traditionellen Tierversuchen oder in vitro-Tests.
Die Bewältigung dieser Herausforderungen erfordert koordinierte Anstrengungen in Materialwissenschaft, Ingenieurwesen, regulatorischer Politik und branchenübergreifender Zusammenarbeit, um das volle Potenzial der Mikrofuidik Organ-on-a-Chip-Technologie zu verwirklichen.
Zukünftige Aussichten: Disruptive Trends, Investitionshotspots und Marktchancen
Die Zukunft der Mikrofuidik Organ-on-a-Chip (OoC) Fertigung steht vor einer signifikanten Transformation, angetrieben von disruptiven technologischen Trends, sich entwickelnden Investitionslandschaften und expandierenden Marktchancen. Da die Nachfrage nach prädiktiveren und menschenrelevanten präklinischen Modellen zunimmt, werden OoC-Plattformen zunehmend als zentrale Werkzeuge in der Wirkstoffforschung, Toxikologie und personalisierten Medizin anerkannt.
Ein besonderer disruptiver Trend ist die Integration von künstlicher Intelligenz (KI) und maschinellem Lernen mit mikrofuidischen OoC-Systemen. Diese Technologien ermöglichen eine Echtzeitanalyse von Daten und prädiktives Modellieren, was die Interpretation komplexer biologischer Reaktionen verbessert und die Optimierung von Chip-Designs beschleunigt. Darüber hinaus ermöglichen Fortschritte in der 3D-Bioprinting- und Biomaterialforschung die Herstellung physiologisch relevanterer Gewebearchitekturen und überbrücken die Kluft zwischen in vitro Modellen und menschlicher Biologie.
Investitionshotspots entstehen in Regionen mit starken Biotechnologie-Ökosystemen und unterstützenden regulatorischen Rahmenbedingungen. Nordamerika, insbesondere die Vereinigten Staaten, bleibt sowohl bei den öffentlichen als auch den privaten Mitteln an der Spitze, mit bedeutenden Initiativen von Institutionen wie den National Institutes of Health und Partnerschaften mit führenden Pharmaunternehmen. Auch Europa verzeichnet ein starkes Wachstum, unterstützt durch den Schwerpunkt der Europäischen Kommission auf Alternativen zu Tierversuchen und die Entwicklung fortschrittlicher Gesundheitstechnologien. In Asien investieren Länder wie Japan und Südkorea stark in Mikrofuidik und regenerative Medizin, was Innovation und Kommerzialisierung fördert.
Marktchancen erweitern sich über die traditionelle pharmazeutische und akademische Forschung hinaus. Die Kosmetikindustrie übernimmt zunehmend OoC-Plattformen, um tierversuchsfreie Vorschriften einzuhalten und die Produktentwicklung zu beschleunigen. Darüber hinaus treibt der Anstieg der personalisierten Medizin die Nachfrage nach patientenspezifischen Chips voran, die maßgeschneiderte Arzneimittel screenings und Krankheitsmodellierungen ermöglichen. Kooperationen zwischen Mikrofuidik-Unternehmen und großen Gesundheitsdienstleistern eröffnen zudem neue Chancen für Diagnostik vor Ort und organspezifische Krankheitsüberwachung.
Mit Blick auf 2025 und darüber hinaus wird erwartet, dass die Konvergenz von Mikrofluidik, fortschrittlichen Materialien und digitalen Gesundheitstechnologien die nächste Innovationswelle in der Organ-on-a-Chip-Produktion katalysiert. Unternehmen und Forschungseinrichtungen, die in skalierbare Fertigung, regulatorische Compliance und interdisziplinäre Partnerschaften investieren, werden gut positioniert sein, um die wachsenden Märkte zu nutzen und die Zukunft der biomedizinischen Forschung und Gesundheitsversorgung zu gestalten.
Anhang: Methodik, Datenquellen und Marktwachstumsprognose (geschätzte CAGR: 18–22 % 2025–2030)
Dieser Anhang skizziert die Methodik, Datenquellen und den Ansatz zur Schätzung der jährlichen Wachstumsrate (CAGR) von 18–22 % für den Markt der Mikrofuidik Organ-on-a-Chip-Produktion von 2025 bis 2030.
- Methodik: Die Schätzung des Marktwachstums basiert auf einer Kombination aus primärer und sekundärer Forschung. Die primäre Forschung umfasste Interviews mit Führungskräften und technischen Experten führender Hersteller von Organ-on-a-Chip, Mikrofuidik-Zulieferern und Endbenutzern in der pharmazeutischen und akademischen Sektoren. Die sekundäre Forschung beinhaltete die Analyse von Jahresberichten, Pressemitteilungen und Produkteinführungen führender Akteure der Branche sowie Daten von Regulierungs- und Normierungsorganisationen.
- Datenquellen: Wichtige Daten stammen aus offiziellen Veröffentlichungen und Mitteilungen großer Unternehmen wie Emulate, Inc., MIMETAS B.V. und CN Bio Innovations Ltd. Zusätzliche Einblicke stammen aus regulatorischen Richtlinien und Förderankündigungen von Organisationen wie den National Institutes of Health (NIH) und der U.S. Food and Drug Administration (FDA). Markttrends wurden mit Daten von Branchenverbänden wie der Microfluidics Association überprüft.
- Marktwachstumsberechnung: Die geschätzte CAGR wurde auf der Grundlage historischer Umsatzdaten (2019–2024) aus den Finanzberichten von Unternehmen berechnet und nach vorn projiziert, basierend auf den erwarteten Akzeptanzraten, Investitionen in Forschung und Entwicklung sowie regulatorischen Entwicklungen. Die Berechnung berücksichtigte auch die zunehmende Anzahl von Partnerschaften zwischen Mikrofuidikunternehmen und Pharmafirmen sowie die Erweiterung der Anwendungen von Organ-on-a-Chip in der Arzneimittelentwicklung und Toxikologietests. Die CAGR-Spanne spiegelt mögliche Variabilitäten in den Marktreferenzen wider, einschließlich technologischer Fortschritte, regulatorischer Akzeptanz und Verfügbarkeit von Mitteln.
- Annahmen und Einschränkungen: Die Prognose geht von einer anhaltenden Investition in Mikrofuidiktechnologien, einer wachsenden Nachfrage nach tierversuchsfreien Testmodellen und unterstützenden regulatorischen Rahmenbedingungen aus. Einschränkungen umfassen mögliche Verzögerungen bei regulatorischen Genehmigungen, Störungen der Lieferkette und unvorhergesehene technologische Herausforderungen.
Diese Methodik gewährleistet einen robusten und transparenten Ansatz zur Marktdimensionierung und Wachstumsprognose für den Sektor der Mikrofuidik Organ-on-a-Chip-Fertigung.
Quellen & Referenzen
- Emulate, Inc.
- MIMETAS B.V.
- ASTM International
- Tissium
- European Medicines Agency (EMA)
- International Organization for Standardization (ISO)
- National Institutes of Health (NIH)
- Europa
- Weltgesundheitsorganisation
- Dolomite Microfluidics
- European Federation of Pharmaceutical Industries and Associations
- Microfluidics Association