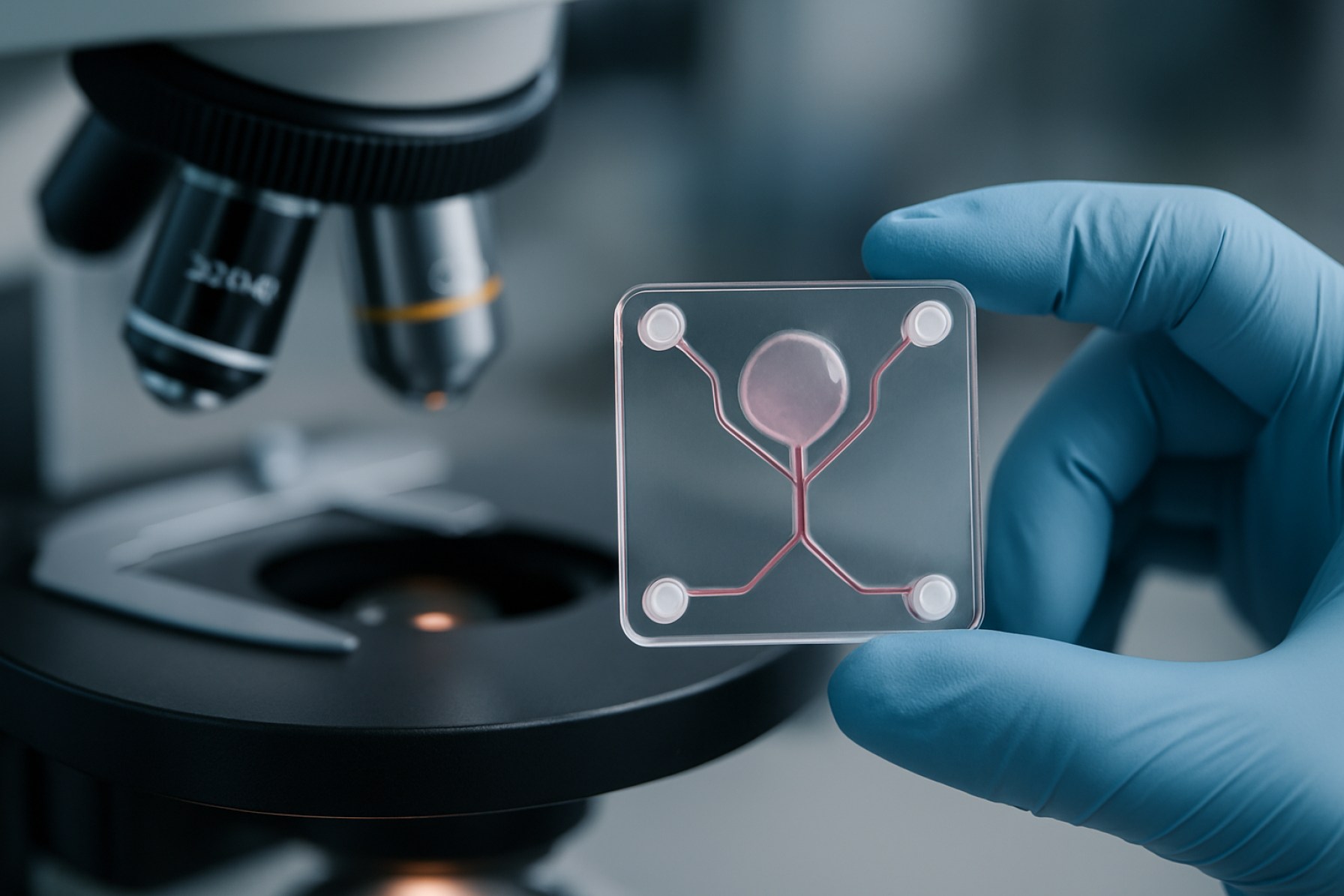
Rewolucja w badaniach biomedycznych: Prognozy na 2025 rok dotyczące wytwarzania mikrofizycznych organów na chipie. Zbadaj przyspieszenie rynku, innowacje technologiczne i przyszłość medycyny precyzyjnej.
- Streszczenie wykonawcze: Kluczowe ustalenia i wyróżnienia na rynku
- Przegląd rynku: Definiowanie wytwarzania mikrofizycznych organów na chipie w 2025 roku
- Wielkość rynku i prognozy (2025–2030): CAGR, prognozy przychodów i czynniki wzrostu
- Krajobraz konkurencyjny: Wiodący gracze, startupy i sojusze strategiczne
- Innowacje technologiczne: Materiały, techniki mikroobróbki i postępy w integracji
- Zastosowania: Odkrywanie leków, toksykologia, modelowanie chorób i medycyna spersonalizowana
- Środowisko regulacyjne i wysiłki na rzecz standaryzacji
- Analiza regionalna: Ameryka Północna, Europa, Azja-Pacyfik i rynki wschodzące
- Wyzwania i bariery: Skalowalność, koszty i przeszkody w przyjęciu
- Perspektywy na przyszłość: Dysrupcyjne trendy, miejsca inwestycji i możliwości rynkowe
- Aneks: Metodologia, źródła danych i obliczenia wzrostu rynku (szacowany CAGR: 18–22% 2025–2030)
- Źródła i odniesienia
Streszczenie wykonawcze: Kluczowe ustalenia i wyróżnienia na rynku
Rynek wytwarzania mikrofizycznych organów na chipie (OoC) ma przed sobą znaczący wzrost w 2025 roku, napędzany postępami w mikroinżynierii, biomateriałach oraz rosnącym popytem na fizjologicznie istotne modele in vitro. Urządzenia organów na chipie, które integrują żywe komórki w systemach mikrofluidycznych, aby symulować funkcje na poziomie organów, rewolucjonizują odkrywanie leków, badania toksykologiczne i modelowanie chorób. Rynek notuje silne inwestycje zarówno ze strony sektora publicznego, jak i prywatnego, a kluczowi gracze, tacy jak Emulate, Inc., MIMETAS B.V. i CN Bio Innovations Ltd prowadzą prace innowacyjne i komercjalizacyjne.
Kluczowe ustalenia wskazują, że adopcja platform OoC w przemyśle farmaceutycznym i biotechnologicznym przyspiesza, głównie dzięki ich zdolności do dostarczania bardziej przewidywalnych danych istotnych dla ludzi w porównaniu do tradycyjnych hodowli komórkowych i modeli zwierzęcych. Agencje regulacyjne, w tym amerykańska Agencja Żywności i Leków (FDA), coraz bardziej doceniają potencjał technologii OoC w ulepszaniu badań przedklinicznych, co dalsze napędza wzrost rynku.
Postępy technologiczne w mikroobróbce – takie jak drukowanie 3D, litografia miękka i zaawansowane materiały polimerowe – umożliwiają produkcję bardziej skomplikowanych i skalowalnych projektów chipów. To ułatwia rozwój chipów wieloorganowych i platform do badań z dużą przepustowością, rozszerzając zakres zastosowań od modeli jednego organu do zintegrowanych systemów człowiek na chipie. Współprace między instytucjami akademickimi, liderami branży a organami regulacyjnymi sprzyjają wysiłkom na rzecz standaryzacji i walidacji, które są kluczowe dla szerszego przyjęcia.
Geograficznie, Ameryka Północna i Europa pozostają na czołowej pozycji w aktywności rynkowej, wspierane przez silną infrastrukturę badawczą i inicjatywy finansowe. Niemniej jednak, Azja-Pacyfik staje się regionem o wysokim wzroście, z rosnącymi inwestycjami w badania biomedyczne i rosnącą obecnością lokalnych producentów.
Podsumowując, rynek wytwarzania mikrofizycznych organów na chipie w 2025 roku charakteryzuje się szybkim postępem technologicznym, rozszerzającymi się obszarami zastosowań i rosnącym akceptacją regulacyjną. Oczekuje się, że te trendy będą napędzać ciągłe inwestycje i innowacje, czyniąc technologie OoC fundamentem next-gen badań biomedycznych i rozwoju leków.
Przegląd rynku: Definiowanie wytwarzania mikrofizycznych organów na chipie w 2025 roku
Wytwarzanie mikrofizycznych organów na chipie reprezentuje transformacyjne podejście w inżynierii biomedycznej, umożliwiające odtworzenie funkcji ludzkich organów na mikroskalowych urządzeniach. Do 2025 roku ta technologia ma odegrać kluczową rolę w odkrywaniu leków, toksykologii i modelowaniu chorób, oferując bardziej fizjologicznie istotne alternatywy dla tradycyjnych hodowli komórkowych i testów na zwierzętach. Sedno systemów organów na chipie tkwi w ich zdolności do integracji żywych komórek w mikrofluidycznych kanałach, symulując dynamiczne mikrośrodowisko ludzkich tkanek i organów.
Rynek wytwarzania mikrofizycznych organów na chipie charakteryzuje się szybkim postępem i rosnącą adopcją w sektorach farmaceutycznym, biotechnologicznym i badaniach akademickich. Kluczowe czynniki wzrostu to popyt na bardziej przewidywalne modele przedkliniczne, potrzeba zmniejszenia uzależnienia od testów na zwierzętach oraz regulacyjne zachęty do alternatywnych metod testowych. W 2025 roku rynek będzie świadkiem zbieżności zaawansowanych materiałów, takich jak biokompatybilne polimery i hydrogeli, z precyzyjnymi technikami mikroobróbki, takimi jak litografia miękka i drukowanie 3D. Te postępy umożliwiają produkcję chipów, które mogą naśladować skomplikowane funkcje organów, w tym unaczynienie, mechaniczne stymulacje i interakcje między organami.
Wiodące organizacje, takie jak Emulate, Inc. i MIMETAS B.V., są na czołowej pozycji, oferując komercyjne platformy wspierające badania z dużą przepustowością i konfigurowalne modele organów. Współprace akademickie i przemysłowe przyspieszają również transfer technologii organów na chipie z laboratorium do rzeczywistych zastosowań, przy czym agencje regulacyjne, takie jak amerykańska Agencja Żywności i Leków (FDA), aktywnie oceniają ich zastosowanie w ocenie bezpieczeństwa i skuteczności leków.
Do 2025 roku krajobraz rynku kształtowany będzie także przez integrację technologii czujników i analityki w czasie rzeczywistym, co pozwoli na ciągłe monitorowanie odpowiedzi komórkowych i warunków mikrośrodowiskowych. Ta zdolność zwiększa wartość systemów organów na chipie w medycynie spersonalizowanej i precyzyjnej terapii. W miarę dojrzewania tej dziedziny, wysiłki na rzecz standaryzacji prowadzone przez organizacje takie jak ASTM International mają ułatwić szersze przyjęcie i interoperacyjność między platformami.
Podsumowując, wytwarzanie mikrofizycznych organów na chipie w 2025 roku definiowane jest przez zaawansowanie technologiczne, rozszerzającą się ofertę komercyjną i rosnącą akceptację regulacyjną, co czyni je fundamentem nowej generacji badań i rozwoju biomedycznego.
Wielkość rynku i prognozy (2025–2030): CAGR, prognozy przychodów i czynniki wzrostu
Globalny rynek wytwarzania mikrofizycznych organów na chipie jest gotowy na znaczny rozwój w latach 2025–2030, napędzany postępami w badaniach biomedycznych, odkrywaniu leków i medycynie spersonalizowanej. Według analiz branżowych rynek ten ma zarejestrować skumulowaną roczną stopę wzrostu (CAGR) na poziomie około 20–25% w tym okresie, a prognozy przychodów osiągną kilka miliardów USD do 2030 roku. Ten dynamiczny wzrost oparty jest na zwiększającym się zapotrzebowaniu na fizjologicznie istotne modele in vitro, które mogą dokładniej odzwierciedlać funkcje ludzkich organów w porównaniu do tradycyjnych hodowli komórkowych lub modeli zwierzęcych.
Kluczowe czynniki wzrostu obejmują rosnącą adopcję platform organów na chipie przez firmy farmaceutyczne i biotechnologiczne w badaniach przedklinicznych i testowaniu toksyczności. Te urządzenia mikrofluidyczne oferują zwiększoną moc przewidywania dla odpowiedzi ludzkich, redukując uzależnienie od testów na zwierzętach i przyspieszając proces rozwoju leków. Ponadto agencje regulacyjne, takie jak amerykańska Agencja Żywności i Leków, coraz częściej dostrzegają wartość technologii organów na chipie w naukach regulacyjnych, co dalej sprzyja ich integracji z przepływami pracy badawczo-rozwojowymi.
Innowacje technologiczne w mikroobróbce, takie jak zaawansowane drukowanie 3D i litografia miękka, również przyspieszają wzrost rynku, umożliwiając produkcję bardziej złożonych i skalowalnych systemów organów na chipie. Wiodące firmy i instytucje badawcze, w tym Emulate, Inc. i CN Bio Innovations, intensywnie inwestują w badania i rozwój, aby rozszerzyć swoje portfele produktów i poprawić powtarzalność oraz wydajność urządzeń.
Geograficznie, Ameryka Północna i Europa mają utrzymać dominujące udziały w rynku, dzięki silnej infrastrukturze badawczej, wsparciu finansowemu oraz obecności kluczowych graczy przemysłowych. Niemniej jednak region Azji-Pacyfiku ma szansę na najszybszy wzrost, z powodu rosnących inwestycji w nauki przyrodnicze i zwiększonego skupienia na innowacyjnych rozwiązaniach zdrowotnych.
Podsumowując, rynek wytwarzania mikrofizycznych organów na chipie jest gotowy na szybki rozwój do 2030 roku, napędzany postępami technologicznymi, wsparciem regulacyjnym oraz urgentną potrzebą bardziej przewidywalnych i etycznych modeli testów przedklinicznych. W miarę dojrzewania tej dziedziny, współprace między akademią, przemysłem i organami regulacyjnymi będą kluczowe dla kształtowania krajobrazu rynku i przyspieszania przyjęcia tych transformacyjnych technologii.
Krajobraz konkurencyjny: Wiodący gracze, startupy i sojusze strategiczne
Krajobraz konkurencyjny wytwarzania mikrofizycznych organów na chipie (OoC) w 2025 roku charakteryzuje się dynamiczną interakcją między ustalonymi liderami branży, innowacyjnymi startupami oraz rosnącą liczbą sojuszy strategicznych. Ten sektor jest napędzany potrzebą bardziej fizjologicznie istotnych modeli in vitro do odkrywania leków, testowania toksyczności i modelowania chorób, co zmusza firmy do innowacji zarówno w zakresie projektowania urządzeń, jak i procesów wytwarzania.
Wśród wiodących graczy, Emulate, Inc. nadal wyznacza standardy swoimi komercjalizowanymi platformami organów na chipie, oferując zestaw chipów, które naśladują ludzkie organy, takie jak płuca, wątroba i jelita. MIMETAS jest kolejnym kluczowym graczem, znanym ze swojej platformy OrganoPlate®, która wykorzystuje technologię mikrofluidyczną do badań z dużą przepustowością i hodowli tkanek 3D. CN Bio Innovations również zdobył uznanie dzięki swojemu systemowi mikrofizjologicznemu z pojedynczymi i wieloma organami, koncentrując się na zastosowaniach w metabolizmie leków i toksyczności.
Ekosystem startupów jest dynamiczny, a firmy takie jak Tissium i Nortis rozwijają nowe techniki wytwarzania i specjalistyczne chipy do niszowych zastosowań, takich jak modele działających tkanek i medycyna spersonalizowana. Te startupy często powstają jako spin-offy akademickie, wykorzystując nowatorskie badania do adresowania specyficznych luk w rynku, takich jak skalowalność, integracja z biosensorami czy kompatybilność z zautomatyzowanymi przepływami pracy.
Sojusze strategiczne coraz bardziej kształtują ten sektor, ponieważ firmy starają się połączyć ekspertyzę w mikroobróbce, biologii komórkowej i analityce danych. Na przykład, Emulate, Inc. nawiązał współpracę z gigantami farmaceutycznymi i organami regulacyjnymi w celu walidacji swoich platform do testów przedklinicznych. Podobnie MIMETAS współpracuje z instytucjami akademickimi i partnerami przemysłowymi w celu rozszerzenia zakresu modeli organów i poprawy wydajności.
Ogólnie rzecz biorąc, krajobraz konkurencyjny w 2025 roku cechuje się szybkim postępem technologicznym, współpracami interdyscyplinarnymi oraz koncentracją na standaryzacji i akceptacji regulacyjnej. To środowisko sprzyja zarówno zdrowej konkurencji, jak i synergicznym partnerstwom, przyspieszając przyjęcie technologii mikrofizycznych organów na chipie w badaniach biomedycznych i rozwoju farmaceutyków.
Innowacje technologiczne: Materiały, techniki mikroobróbki i postępy w integracji
Ostatnie lata przyniosły znaczące innowacje technologiczne w wytwarzaniu mikrofizycznych organów na chipie (OoC), napędzane potrzebą uzyskania bardziej fizjologicznie istotnych modeli in vitro. Postępy w naukach materiałowych poszerzyły zakres podłoży poza tradycyjny polidimetylosiloksan (PDMS), rozwiązując problemy takie jak absorpcja małych cząsteczek i ograniczona skalowalność. Termoplasty, takie jak kopolimer cyklicznego olefinu (COC) i polimetakrylan metylu (PMMA), zyskują coraz większe uznanie za swoje właściwości optyczne, biokompatybilność i możliwość masowej produkcji poprzez formowanie wtryskowe. Dodatkowo, hydrogeli i bioaktywne polimery są projektowane w celu lepszego naśladowania macierzy pozakomórkowej, wspierając bardziej złożone architektury tkanek i dynamiczne interakcje komórkowe.
Techniki mikroobróbki również ewoluowały, przechodząc od konwencjonalnej litografii miękkiej do bardziej wszechstronnych i skalowalnych metod. Wysoka rozdzielczość druku 3D, w tym polimeryzacja dwupromieniowa i przetwarzanie światłem cyfrowym, umożliwia szybkie prototypowanie skomplikowanych sieci mikrokanalizacyjnych i struktury wielowarstwowe. Mikroobróbka laserowa i gorące tłoczenie dalej zwiększają precyzję i wydajność produkcji urządzeń. Te techniki umożliwiają integrację wielu rodzajów komórek, sieci naczyniowych i mechanicznych elementów aktywacyjnych w jednym chipie, dokładnie naśladując funkcje na poziomie organów.
Postępy w integracji są kluczowe dla nowej generacji platform OoC. Włączenie zintegrowanych czujników – takich jak elektrody do odczytów elektrycznych, czujniki optyczne do obrazowania w czasie rzeczywistym i mikrofluidyczne zawory do dynamicznej kontroli przepływu – umożliwia ciągłe monitorowanie odpowiedzi komórkowych i warunków otoczenia. Modułowe strategie projektowe pozwalają na połączenie kilku chipów organowych, wspierając systemy wieloorganowe lub „ciało na chipie”, które lepiej symulują interakcje systemiczne. Co więcej, przyjęcie standardowych interfejsów i sprzętu open-source promuje interoperacyjność i powtarzalność wśród grup badawczych i partnerów przemysłowych.
Te innowacje technologiczne są wspierane przez współprace między instytucjami akademickimi, liderami branży a organami regulacyjnymi. Na przykład, Emulate, Inc. i MIMETAS B.V. wprowadzają na rynek komercyjne platformy OoC z zaawansowanymi materiałami i funkcjami integracyjnymi, podczas gdy organizacje takie jak amerykańska Agencja Żywności i Leków (FDA) aktywnie oceniają te technologie pod kątem akceptacji regulacyjnej. W miarę dojrzewania tych innowacji oczekuje się, że przyspieszą one przyjęcie systemów OoC w rozwoju leków, modelowaniu chorób i medycynie spersonalizowanej.
Zastosowania: Odkrywanie leków, toksykologia, modelowanie chorób i medycyna spersonalizowana
Mikrofizyczne platformy organów na chipie (OoC) szybko rozwijają dziedziny odkrywania leków, toksykologii, modelowania chorób i medycyny spersonalizowanej, dostarczając fizjologicznie istotnych modeli in vitro, które rekapituluują funkcje ludzkich organów. Te systemy mikroinżynieryjne, wytwarzane za pomocą technik takich jak litografia miękka, drukowanie 3D i fotolitografia, umożliwiają precyzyjną kontrolę nad mikrośrodowiskami komórkowymi, przepływem cieczy i interfejsami tkankowymi, co jest kluczowe dla naśladowania złożoności ludzkich organów.
W odkrywaniu leków, urządzenia OoC umożliwiają badania przesiewowe z dużą przepustowością substancji farmaceutycznych w warunkach zbliżonych do fizjologii ludzkiej. To zmniejsza uzależnienie od modeli zwierzęcych i tradycyjnych kultur komórkowych, które często nie potrafią dokładnie przewidzieć odpowiedzi ludzi. Na przykład, systemy wątroba na chipie i serce na chipie były używane do oceny metabolizmu leków i kardiotoksyczności, dostarczając wczesnych informacji na temat profili skuteczności i bezpieczeństwa. Firmy takie jak Emulate, Inc. i MIMETAS B.V. opracowały komercyjne platformy, które są coraz częściej stosowane przez firmy farmaceutyczne do testów przedklinicznych.
Badania toksykologiczne korzystają z technologii OoC, umożliwiając ocenę wpływu substancji chemicznych i toksyn środowiskowych na ludzkie tkanki. Modele płuca na chipie i nerki na chipie, na przykład, były nieocenione w ocenie wpływu zanieczyszczeń powietrza i leków nefrotoksycznych. Te systemy zapewniają monitorowanie w czasie rzeczywistym odpowiedzi komórkowych, integralności bariery i przeżywalności tkanek, oferując bardziej przewidywalną i etyczną alternatywę dla testów na zwierzętach. Agencje regulacyjne, w tym amerykańska Agencja Żywności i Leków, aktywnie badają integrację danych OoC w procesach oceny bezpieczeństwa.
Modelowanie chorób to kolejna transformacyjna aplikacja, w której platformy OoC są używane do odtworzenia patologicznych warunków, takich jak nowotwory, choroby neurodegeneracyjne i choroby zakaźne. Poprzez włączenie komórek pochodzących od pacjentów, badacze mogą badać postęp choroby, interakcje między gospodarzem a patogenem oraz odpowiedzi terapeutyczne w kontrolowanym mikrośrodowisku. To podejście okazało się szczególnie cenne w modelowaniu rzadkich chorób i zrozumieniu mechanizmów, które trudno uchwycić in vivo.
Medycyna spersonalizowana ma szansę znacznie skorzystać na technologii OoC. Integrując komórki specyficzne dla pacjenta w chipy organowe, możliwe jest przewidywanie indywidualnych reakcji na leki i dostosowywanie terapii. To spersonalizowane podejście jest badane przez organizacje takie jak CN Bio Innovations, które opracowują systemy wątroby na chipie do zastosowań w medycynie precyzyjnej. W miarę jak techniki wytwarzania nadal się rozwijają, skalowalność i powtarzalność urządzeń OoC ma szansę jeszcze bardziej zwiększyć ich wpływ w badaniach biomedycznych i praktyce klinicznej.
Środowisko regulacyjne i wysiłki na rzecz standaryzacji
Środowisko regulacyjne i wysiłki na rzecz standaryzacji związane z wytwarzaniem mikrofizycznych organów na chipie (OoC) szybko się rozwijają, gdy te technologie przechodzą z badań akademickich do zastosowań komercyjnych i klinicznych. Agencje regulacyjne, takie jak amerykańska Agencja Żywności i Leków (FDA) oraz Europejska Agencja Leków (EMA), coraz bardziej angażują interesariuszy w celu opracowania ram zapewniających bezpieczeństwo, niezawodność i powtarzalność urządzeń OoC. Agencje te uznają potencjał systemów OoC do zmniejszenia uzależnienia od testów na zwierzętach oraz poprawy mocy przewidywania przedklinicznych ocen leków.
Kluczowym wyzwaniem w krajobrazie regulacyjnym jest brak powszechnie akceptowanych standardów dotyczących projektowania, wytwarzania i walidacji mikrofluidycznych platform OoC. W celu rozwiązania tego problemu, organizacje takie jak ASTM International i Międzynarodowa Organizacja Normalizacyjna (ISO) zainicjowały grupy robocze skupiające się na opracowaniu standardów konsensusu dotyczących materiałów, wydajności urządzeń i walidacji biologicznej. Te działania mają na celu harmonizację protokołów testowych, raportowania danych i miar kontroli jakości, co ułatwi akceptację regulacyjną i powtarzalność między laboratoriami.
W 2025 roku współprace między przemysłem, nauką a organami regulacyjnymi przyspieszają ustanawianie najlepszych praktyk. Na przykład, National Centre for the Replacement, Refinement and Reduction of Animals in Research (NC3Rs) w Wielkiej Brytanii aktywnie wspiera rozwój wytycznych walidacji OoC, aby zapewnić, że modele te można wiarygodnie stosować w zgłoszeniach regulacyjnych. Podobnie, Narodowe Instytuty Zdrowia (NIH) w Stanach Zjednoczonych finansują konsorcja, które koncentrują się na standaryzacji procesów wytwarzania i biologicznych punktów końcowych dla systemów OoC.
Pomimo tych postępów, nadal istnieją wyzwania związane z dostosowaniem globalnych wymagań regulacyjnych i zapewnieniem, że standardy nadążają za szybkim rozwojem technologicznym. Kontynuacja dialogu między producentami urządzeń, użytkownikami końcowymi a regulatorami jest niezbędna w celu rozwiązania takich kwestii jak skalowalność urządzeń, integracja z istniejącymi przepływami pracy laboratoryjnej i długoterminowa biokompatybilność. W miarę dojrzewania wysiłków na rzecz standaryzacji oczekuje się, że uproszczą one ścieżkę do uzyskania zgody regulacyjnej, sprzyjając wzrostowi branży i w końcu zwiększając wpływ technologii mikrofizycznych organów na chipie w badaniach biomedycznych i rozwoju leków.
Analiza regionalna: Ameryka Północna, Europa, Azja-Pacyfik i rynki wschodzące
Globalny krajobraz wytwarzania mikrofizycznych organów na chipie (OoC) charakteryzuje się znacznymi różnicami regionalnymi w intensywności badań, komercjalizacji oraz strukturach regulacyjnych. W Ameryce Północnej, szczególnie w Stanach Zjednoczonych, sektor ten jest napędzany przez solidne finansowanie ze strony agencji takich jak Narodowe Instytuty Zdrowia oraz silny ekosystem partnerstw między uczelniami a przemysłem. Wiodące uniwersytety i startupy współpracują, aby zwiększyć złożoność chipów i ich wydajność, koncentrując się na zastosowaniach w odkrywaniu leków i toksykologii. Obecność dużych firm farmaceutycznych oraz sprzyjające środowisko regulacyjne dalej przyspieszają adopcję technologii OoC.
W Europie nacisk kładziony jest na standaryzację, współprace transgraniczne oraz rozważania etyczne. Program Horyzont Europa Unii Europejskiej finansuje projekty międzynarodowe mające na celu ujednolicenie protokołów wytwarzania oraz integrację platform OoC w przepływach testów przedklinicznych. Kraje takie jak Niemcy, Holandia i Wielka Brytania tworzą ośrodki innowacji, w których firmy i instytuty badawcze pracują nad rozwiązaniem problemów związanych ze skalowalnością i powtarzalnością. Agencje regulacyjne w Europie również aktywnie angażują się w dialog z interesariuszami przemysłowymi w celu opracowania wytycznych dotyczących walidacji i akceptacji danych OoC w zgłoszeniach regulacyjnych.
Region Azji-Pacyfiku, prowadzony przez Chiny, Japonię i Singapur, doświadcza szybkiego wzrostu w wytwarzaniu mikrofizycznych OoC. Rządy mocno inwestują w infrastrukturę biotechnologiczną, a instytucje akademickie produkują badania o wysokim wpływie na nowatorskie materiały chipowe oraz technologie czujników zintegrowanych. Ekspertyza produkcyjna w regionie umożliwia efektywną kosztowo produkcję i szybkie prototypowanie, co czyni Azję-Pacyfik kluczowym graczem w globalnym łańcuchu dostaw komponentów mikrofluidycznych. Strategiczne partnerstwa między lokalnymi firmami a globalnymi firmami farmaceutycznymi również sprzyjają transferowi technologii oraz ekspansji rynku.
Rynki wschodzące w Ameryce Łacińskiej, na Bliskim Wschodzie i w Afryce stopniowo wkraczają na obszar OoC, głównie poprzez współprace akademickie i projekty pilotażowe. Chociaż infrastruktura i finansowanie pozostają ograniczone w porównaniu do ugruntowanych regionów, inicjatywy wspierane przez organizacje takie jak Światowa Organizacja Zdrowia pomagają budować lokalne zdolności. Rynki te mają szansę skorzystać na transferze technologii i dostosowaniu platform OoC do regionalnych wyzwań zdrowotnych, takich jak modelowanie chorób zakaźnych i toksykologia środowiskowa.
Ogólnie rzecz biorąc, dynamika regionalna w wytwarzaniu mikrofizycznych organów na chipie odzwierciedla różne priorytety, od innowacji i komercjalizacji w Ameryce Północnej i Azji-Pacyfiku do standaryzacji i etycznego nadzoru w Europie, przy jednoczesnym stopniowym integrowaniu rynków wschodzących w globalny ekosystem.
Wyzwania i bariery: Skalowalność, koszty i przeszkody w przyjęciu
Pomimo znaczących postępów w technologii mikrofizycznych organów na chipie (OoC), kilka wyzwań utrudnia jej szeroką akceptację i skalowalność przemysłową. Jedną z głównych barier jest złożoność procesów produkcji. Większość urządzeń OoC produkowana jest za pomocą litografii miękkiej z polidimetylosiloksanu (PDMS), metody, która, choć precyzyjna, jest pracochłonna i trudna do skalowania do masowej produkcji. Przejście na alternatywne materiały i techniki produkcji, takie jak termoplasty i formowanie wtryskowe, jest w toku, ale wymaga znacznych inwestycji w nową infrastrukturę i optymalizację procesów (Dolomite Microfluidics).
Koszt pozostaje istotną przeszkodą. Wysoka cena niestandardowej mikroobróbki, specjalistycznych materiałów oraz potrzeba wykwalifikowanego personelu przyczyniają się do ogólnych kosztów urządzeń OoC. To ogranicza dostępność dla mniejszych laboratoriów badawczych i spowalnia tempo innowacji. Ponadto integracja wielu rodzajów komórek i odtwarzanie skomplikowanych interfejsów tkankowych na jednym chipie zwiększa zarówno trudność techniczną, jak i koszty produkcji (Emulate, Inc.).
Przyjęcie technologii jest również utrudnione przez braki w standaryzacji w branży. Zmienność w projektowaniu urządzeń, materiałach i protokołach sprawia, że trudne jest porównanie wyników między badaniami lub walidacja modeli OoC do celów regulacyjnych. Agencje regulacyjne, takie jak amerykańska Agencja Żywności i Leków, współpracują z interesariuszami branżowymi w celu opracowania wytycznych, ale harmonizacja jest wciąż w toku. Ponadto integracja platform OoC w istniejące procesy rozwoju leków wymaga znacznych zmian w przepływach pracy i zarządzaniu danymi, co może być odstraszające dla ugruntowanych firm farmaceutycznych (Europejska Federacja Przemysłu i Stowarzyszeń Farmaceutycznych).
Na koniec, biologiczna złożoność ludzkich organów jest trudna do całkowitego odtworzenia na chipie. Osiągnięcie długoterminowej przeżywalności komórek, funkcjonalnych interfejsów tkankowych oraz fizjologicznie istotnych odpowiedzi pozostaje wyzwaniem technicznym. Te ograniczenia wpływają na moc przewidywania modeli OoC i ich akceptację jako alternatyw dla tradycyjnych testów na zwierzętach lub badań in vitro.
Rozwiązanie tych wyzwań wymaga skoordynowanych wysiłków w naukach materiałowych, inżynierii, polityce regulacyjnej oraz współpracy przemysłowej, aby w pełni zrealizować potencjał technologii mikrofizycznych organów na chipie.
Perspektywy na przyszłość: Dysrupcyjne trendy, miejsca inwestycji i możliwości rynkowe
Przyszłość wytwarzania mikrofizycznych organów na chipie (OoC) jest gotowa na znaczną transformację, napędzaną dysrupcyjnymi trendami technologicznymi, ewoluującym krajobrazem inwestycyjnym i rozszerzającymi się możliwościami rynkowymi. W miarę jak zapotrzebowanie na bardziej przewidywalne i fizjologicznie istotne modele przedkliniczne narasta, platformy OoC są coraz bardziej doceniane jako kluczowe narzędzia w odkrywaniu leków, toksykologii i medycynie spersonalizowanej.
Jednym z najbardziej dysrupcyjnych trendów jest integracja sztucznej inteligencji (AI) oraz uczenia maszynowego z systemami mikrofluidycznymi OoC. Te technologie umożliwiają analizę danych w czasie rzeczywistym oraz modelowanie predykcyjne, wzmacniając interpretację złożonych odpowiedzi biologicznych i przyspieszając optymalizację projektów chipów. Dodatkowo postępy w drukowaniu 3D i biomateriałach pozwalają na wytwarzanie bardziej fizjologicznie istotnych architektur tkanek, co further zmniejsza różnice między modelami in vitro a biologią ludzką.
Miejsca inwestycji pojawiają się w regionach z silnymi ekosystemami biotechnologicznymi i sprzyjającymi ramami regulacyjnymi. Ameryka Północna, szczególnie Stany Zjednoczone, nadal prowadzi zarówno w publicznym, jak i prywatnym finansowaniu, z znacznymi inicjatywami ze strony agencji takich jak Narodowe Instytuty Zdrowia oraz partnerstw z wiodącymi firmami farmaceutycznymi. Europa również doświadcza solidnego wzrostu, wspierana przez nacisk Komisji Europejskiej na alternatywy dla testów na zwierzętach i rozwój zaawansowanych technologii opieki zdrowotnej. W Azji kraje takie jak Japonia i Korea Południowa intensywnie inwestują w mikrofluidykę i medycynę regeneracyjną, sprzyjając innowacjom i komercjalizacji.
Możliwości rynkowe rozszerzają się poza tradycyjne badania farmaceutyczne i akademickie. Przemysł kosmetyczny coraz częściej przyjmuje platformy OoC, aby dostosować się do zakazów testów na zwierzętach i przyspieszyć rozwój produktów. Ponadto, rosnąca medycyna spersonalizowana napędza zapotrzebowanie na chipy specyficzne dla pacjenta, umożliwiające dostosowane badania przesiewowe leków i modelowanie chorób. Współprace między firmami mikrofluidycznymi a dużymi dostawcami opieki zdrowotnej otwierają także nowe możliwości w diagnostyce punktowej i monitorowaniu chorób specyficznych dla organów.
Patrząc w przyszłość na 2025 rok i dalej, zbieżność mikrofluidyki, zaawansowanych materiałów i technologii zdrowia cyfrowego ma szansę pobudzić następna falę innowacji w wytwarzaniu organów na chipie. Firmy i instytucje badawcze, które inwestują w skalowalną produkcję, zgodność z regulacjami oraz współprace międzydyscyplinarne, będą dobrze przygotowane do czerpania korzyści z rosnącego rynku i kształtowania przyszłości badań biomedycznych i opieki zdrowotnej.
Aneks: Metodologia, źródła danych i obliczenia wzrostu rynku (szacowany CAGR: 18–22% 2025–2030)
Ten aneks przedstawia metodologię, źródła danych i podejście użyte do oszacowania skumulowanej rocznej stopy wzrostu (CAGR) na poziomie 18–22% dla rynku wytwarzania mikrofizycznych organów na chipie w latach 2025–2030.
- Metodologia: Szacowanie wzrostu rynku opiera się na połączeniu badań pierwotnych i wtórnych. Badania pierwotne obejmowały wywiady z kierownikami i ekspertami technicznymi w wiodących firmach produkujących organy na chipie, dostawcami mikrofluidyki oraz użytkownikami końcowymi w sektorze farmaceutycznym i akademickim. Badania wtórne obejmowały analizę raportów rocznych, komunikatów prasowych i wprowadzania produktów przez kluczowych graczy branżowych, a także dane z organizacji regulacyjnych i standardowych.
- Źródła danych: Kluczowe dane pozyskano z oficjalnych publikacji i komunikacji głównych firm, takich jak Emulate, Inc., MIMETAS B.V. i CN Bio Innovations Ltd. Dodatkowe informacje pozyskano z wytycznych regulacyjnych i ogłoszeń o finansowaniu przez takie organizacje jak Narodowe Instytuty Zdrowia (NIH) oraz amerykańska Agencja Żywności i Leków (FDA). Trendy rynkowe były weryfikowane na podstawie danych z towarzystw branżowych, takich jak Stowarzyszenie Mikrofluidyki.
- Obliczenia wzrostu rynku: Oszacowany CAGR obliczono na podstawie danych o przychodach historycznych (2019–2024) z raportów finansowych firm i projetkowano na przyszłość w oparciu o przewidywane stopy adopcji, inwestycje w badania i rozwój oraz rozwój regulacyjny. Obliczenia uwzględniały także rosnącą liczbę partnerstw między firmami mikrofluidycznymi a firmami farmaceutycznymi, a także rozszerzanie zastosowań organów na chipie w odkrywaniu leków i badaniach toksykologicznych. Zakres CAGR odzwierciedla potencjalną zmienność w czynnikach sterujących rynkiem, w tym postępów technologicznych, akceptacji regulacyjnej i dostępności finansowania.
- Założenia i ograniczenia: Prognoza zakłada ciągłe inwestycje w technologie mikrofluidyczne, rosnące zapotrzebowanie na modele testowe bez udziału zwierząt oraz sprzyjające ramy regulacyjne. Ograniczenia obejmują potencjalne opóźnienia w uzyskiwaniu zgód regulacyjnych, zakłócenia w łańcuchach dostaw i nieprzewidziane wyzwania technologiczne.
Metodologia ta zapewnia solidne i przejrzyste podejście do określenia wielkości rynku i oszacowań wzrostu sektora wytwarzania mikrofizycznych organów na chipie.
Źródła i odniesienia
- Emulate, Inc.
- MIMETAS B.V.
- ASTM International
- Tissium
- Europejska Agencja Leków (EMA)
- Międzynarodowa Organizacja Normalizacyjna (ISO)
- Narodowe Instytuty Zdrowia (NIH)
- Europa
- Światowa Organizacja Zdrowia
- Dolomite Microfluidics
- Europejska Federacja Przemysłu i Stowarzyszeń Farmaceutycznych
- Stowarzyszenie Mikrofluidyki