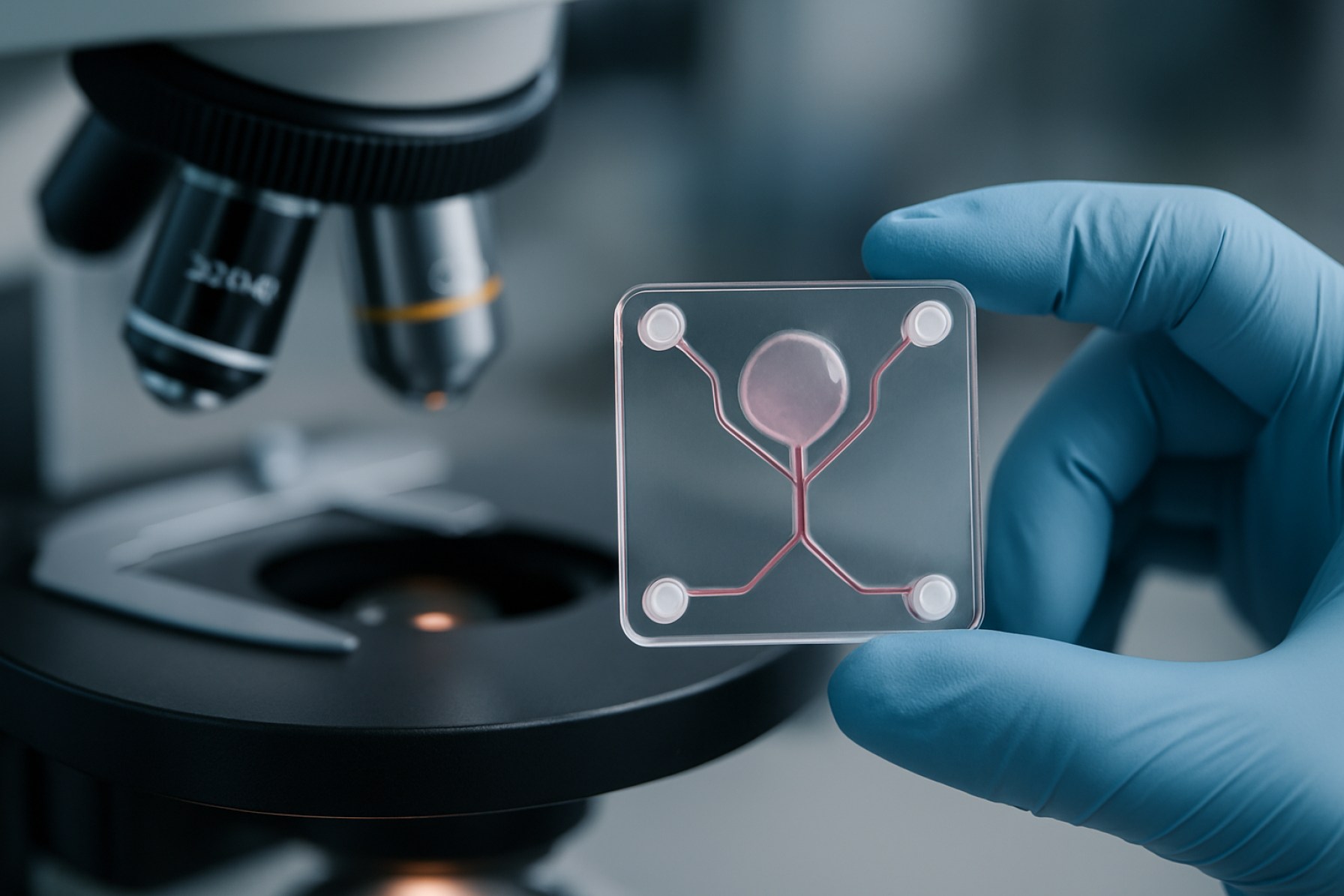
Revolutionerende biomedicinsk forskning: Udsigt til 2025 for mikrofluidisk organ-on-a-chip fremstilling. Udforsk markedsaccelerationen, teknologiske innovationer og fremtiden for præcisionsmedicin.
- Sammendrag: Nøglefund og markedsfokus
- Markedsoversigt: Definition af mikrofluidisk organ-on-a-chip fremstilling i 2025
- Markedsstørrelse og prognose (2025–2030): CAGR, indtægtsprognoser og vækstdrivere
- Konkurrencebillede: Ledende spillere, startups og strategiske alliancer
- Technologiske innovationer: Materialer, mikroproduktionsmetoder og integrationsfremskridt
- Anvendelser: Lægemiddelopdagelse, toksikologi, sygdomsmodellering og personlig medicin
- Regulatorisk miljø og standardiseringsbestræbelser
- Regional analyse: Nordamerika, Europa, Asien-Stillehavsområdet og vækstmarkeder
- Udfordringer og barrierer: Skalerbarhed, omkostninger og vedtagelsesvanskeligheder
- Fremtidsudsigter: Disruptive tendenser, investeringshotspots og markedsmuligheder
- Appendiks: Metodologi, datakilder og markedsvækstberegning (Estimeret CAGR: 18–22% 2025–2030)
- Kilder & Referencer
Sammendrag: Nøglefund og markedsfokus
Markedet for mikrofluidisk organ-on-a-chip (OoC) fremstilling er klar til betydelig vækst i 2025, drevet af fremskridt inden for mikroengineering, biomaterialer og den stigende efterspørgsel efter fysiologisk relevante in vitro-modeller. Organ-on-a-chip-enheder, der integrerer levende celler i mikrofluidiske systemer for at simulere organ-niveau funktioner, revolutionerer lægemiddelopdagelse, toksikologitestning og sygdomsmodellering. Markedet oplever stærke investeringer fra både offentlige og private sektorer, hvor nøglespillere som Emulate, Inc., MIMETAS B.V. og CN Bio Innovations Ltd fører an i innovations- og kommercialiseringsindsatserne.
Nøglefund viser, at adoptionen af mikrofluidiske OoC-platforme accelererer i farmaceutiske og bioteknologiske industrier, primært på grund af deres evne til at give mere prædiktive menneske-relevante data sammenlignet med traditionelle cellekulturer og dyremodeller. Regulerende myndigheder, herunder den amerikanske Food and Drug Administration (FDA), anerkender i stigende grad potentialet i OoC-teknologier til at forbedre præklinisk testning, hvilket yderligere fremmer markedsvæksten.
Teknologiske fremskridt inden for mikroproduktion – såsom 3D-print, blød lithografi og avancerede polymermaterialer – muliggør produktionen af mere komplekse og skalerbare chipdesigns. Dette letter udviklingen af multi-organ chips og højgennemstrømningsscreeningplatforme, hvilket udvider anvendelsesområdet fra enkelt-organ modeller til integrerede menneske-på-chip systemer. Samarbejder mellem akademiske institutioner, brancheledere og regulerende organer fremmer standardisering og valideringsindsatser, som er kritiske for bredere adoption.
Geografisk set forbliver Nordamerika og Europa i front for markedsaktiviteter, understøttet af stærk forskningsinfrastruktur og finansieringsinitiativer. Dog vokser Asien-Stillehavet frem som et højvækstområde med stigende investeringer i biomedicinsk forskning og en voksende tilstedeværelse af lokale producenter.
Sammenfattende er markedet for mikrofluidisk organ-on-a-chip fremstilling i 2025 præget af hurtige teknologiske fremskridt, udvidende anvendelsesområder og voksende regulatorisk accept. Disse tendenser forventes at drive fortsatte investeringer og innovation, hvilket positionerer OoC-teknologier som en hjørnesten i næste generations biomedicinsk forskning og lægemiddeludvikling.
Markedsoversigt: Definition af mikrofluidisk organ-on-a-chip fremstilling i 2025
Mikrofluidisk organ-on-a-chip fremstilling repræsenterer en transformativ tilgang inden for biomedicinsk engineering, der muliggør rekonstruktionen af menneskelige organfunktioner på mikroskala enheder. Inden 2025 forventes denne teknologi at spille en afgørende rolle i lægemiddelopdagelse, toksikologi og sygdomsmodellering, idet den tilbyder mere fysiologisk relevante alternativer til traditionelle cellekulturer og dyreforsøg. Kernen i organ-on-a-chip systemer ligger i deres evne til at integrere levende celler i mikrofluidiske kanaler, hvilket simulerer det dynamiske mikromiljø af menneskelige væv og organer.
Markedet for mikrofluidisk organ-on-a-chip fremstilling er præget af hurtig innovation og stigende adoption på tværs af farmaceutiske, bioteknologiske og akademiske forskningssektorer. Nøgledrivere inkluderer efterspørgslen efter mere prædiktive prækliniske modeller, behovet for at reducere afhængigheden af dyreforsøg og regulatorisk opmuntring til alternative testmetoder. I 2025 oplever markedet konvergensen af avancerede materialer, såsom biokompatible polymerer og hydrogeler, med præcisions mikroproduktionsmetoder som blød lithografi og 3D-print. Disse fremskridt muliggør produktionen af chips, der kan efterligne komplekse organ-niveau funktioner, herunder vaskularisering, mekanisk stimulering og multi-organ interaktioner.
Førende organisationer som Emulate, Inc. og MIMETAS B.V. er i front, og tilbyder kommercielle platforme, der understøtter højgennemstrømningsscreening og tilpassede organmodeller. Akademiske og industrielle samarbejder fremskynder yderligere oversættelsen af organ-on-a-chip teknologier fra laboratoriet til virkelige anvendelser, hvor regulatoriske organer som den amerikanske Food and Drug Administration (FDA) aktivt evaluerer deres brug i sikkerheds- og effektvurderinger af lægemidler.
I 2025 er markedets landskab også præget af integrationen af sensorteknologier og realtidsanalyse, hvilket muliggør kontinuerlig overvågning af cellulære responser og mikromiljøbetingelser. Denne funktion forbedrer værdiforholdet af organ-on-a-chip systemer for personlig medicin og præcisions terapeutik. Efterhånden som feltet modnes, forventes standardiseringsindsatser ledet af organisationer såsom ASTM International at fremme bredere adoption og interoperabilitet på tværs af platforme.
Sammenfattende defineres mikrofluidisk organ-on-a-chip fremstilling i 2025 ved teknologisk sofistikering, ekspanderende kommercielle tilbud og voksende regulatorisk accept, hvilket positionerer den som en hjørnesten i næste generations biomedicinsk forskning og udvikling.
Markedsstørrelse og prognose (2025–2030): CAGR, indtægtsprognoser og vækstdrivere
Det globale marked for mikrofluidisk organ-on-a-chip fremstilling er klar til betydelig ekspansion mellem 2025 og 2030, drevet af fremskridt i biomedicinsk forskning, lægemiddelopdagelse og personlig medicin. Ifølge brancheanalyser forventes markedet at registrere en samlet årlig vækst (CAGR) på cirka 20–25% i denne periode, med indtægtsprognoser, der når flere milliarder USD inden 2030. Denne robuste vækst er understøttet af den stigende efterspørgsel efter fysiologisk relevante in vitro-modeller, der kan reproducere menneskelige organfunktioner mere nøjagtigt end traditionelle cellekulturer eller dyremodeller.
Nøglevækstdrivere inkluderer den stigende adoption af organ-on-a-chip platforme blandt farmaceutiske og bioteknologiske virksomheder til præklinisk lægemiddel screening og toksikologitest. Disse mikrofluidiske enheder tilbyder forbedret prædiktiv power for menneskelige reaktioner, hvilket reducerer afhængigheden af dyreforsøg og accelererer lægemiddeludviklingsprocessen. Desuden anerkender regulatoriske myndigheder som den amerikanske Food and Drug Administration i stigende grad værdien af organ-on-a-chip teknologier inden for regulatorisk videnskab, hvilket yderligere tilskynder deres integration i forsknings- og udviklingsarbejdsprocesser.
Teknologiske innovationer i mikroproduktion, såsom avanceret 3D-print og blød lithografi, driver også markedsvæksten ved at muliggøre produktionen af mere komplekse og skalerbare organ-on-a-chip systemer. Førende virksomheder og forskningsinstitutter, herunder Emulate, Inc. og CN Bio Innovations, investerer kraftigt i F&U for at udvide deres produktporteføljer og forbedre enhedens reproducerbarhed og gennemstrømning.
Geografisk set forventes Nordamerika og Europa at opretholde dominerende markedsandele på grund af stærk forskningsinfrastruktur, finansieringsstøtte og tilstedeværelsen af nøglespillere i branchen. Imidlertid forventes Asien-Stillehavsområdet at opleve den hurtigste vækst, drevet af stigende investeringer i livsvidenskab og et voksende fokus på innovative sundhedsløsninger.
Sammenfattende er markedet for mikrofluidisk organ-on-a-chip fremstilling indstillet på hurtig ekspansion indtil 2030, drevet af teknologiske fremskridt, regulatorisk støtte og det presserende behov for mere prædiktive og etiske prækliniske testmodeller. Efterhånden som feltet modnes, vil samarbejdet mellem akademia, industri og regulerende organer være afgørende for at forme markedets landskab og fremskynde adoptionen af disse transformative teknologier.
Konkurrencebillede: Ledende spillere, startups og strategiske alliancer
Det konkurrenceprægede billede for mikrofluidisk organ-on-a-chip (OoC) fremstilling i 2025 er præget af et dynamisk samspil mellem etablerede brancheledere, innovative startups og et voksende antal strategiske alliancer. Denne sektor drives af behovet for mere fysiologisk relevante in vitro-modeller til lægemiddelopdagelse, toksikologitestning og sygdomsmodellering, hvilket presser virksomheder til at innovere både enheddesign og fremstillingsprocesser.
Blandt de førende spillere fortsætter Emulate, Inc. med at sætte standarder med sine kommercialiserede organ-on-a-chip platforme, der tilbyder en række chips, der efterligner menneskelige organer såsom lunger, lever og tarm. MIMETAS er en anden vigtig aktør, kendt for sin OrganoPlate® platform, som udnytter mikrofluidisk teknologi til højgennemstrømningsscreening og 3D vævskultur. CN Bio Innovations har også etableret sig med single- og multi-organ mikro fysiologiske systemer, med fokus på anvendelser i lægemiddelmetabolisme og toksicitet.
Startup-økosystemet er livligt, med virksomheder som Tissium og Nortis, der udvikler nye fremstillingsteknikker og specialiserede chips til nicheanvendelser, såsom vaskulariserede vævsmodeller og personlig medicin. Disse startups opstår ofte fra akademiske spin-offs, der udnytter banebrydende forskning til at adressere specifikke huller i markedet, såsom skalerbarhed, integration med biosensorer eller kompatibilitet med automatiserede arbejdsprocesser.
Strategiske alliancer former i stigende grad sektoren, da virksomheder søger at kombinere ekspertise inden for mikroproduktion, cellebiologi og dataanalyse. For eksempel har Emulate, Inc. samarbejdet med store farmaceutiske virksomheder og regulatoriske organer for at validere sine platforme til præklinisk testning. Tilsvarende samarbejder MIMETAS med akademiske institutioner og industrier for at udvide mængden af organmodeller og forbedre gennemstrømning.
Overordnet set er det konkurrenceprægede billede i 2025 præget af hurtige teknologiske fremskridt, tværfaglige samarbejder og fokus på standardisering og regulatorisk accept. Dette miljø fremmer både sund konkurrence og synergistiske partnerskaber, hvilket accelererer adoptionen af mikrofluidiske organ-on-a-chip teknologier i biomedicinsk forskning og farmaceutisk udvikling.
Technologiske innovationer: Materialer, mikroproduktionsmetoder og integrationsfremskridt
De seneste år har været vidne til betydelige teknologiske innovationer inden for fremstillingen af mikrofluidiske organ-on-a-chip (OoC) enheder, drevet af behovet for mere fysiologisk relevante in vitro-modeller. Fremskridt inden for materialeforskning har udvidet rækken af substrater udover traditionelle polydimethylsiloxan (PDMS) for at tackle problemer som absorption af små molekyler og begrænset skalerbarhed. Termoplastikker som cyklisk olefin co-polymer (COC) og polymethylmethacrylate (PMMA) anvendes i stigende grad på grund af deres optiske klarhed, biokompatibilitet og egnethed til masseproduktion gennem injektionsstøbning. Derudover udvikles hydrogeler og bioaktive polymerer for bedre at efterligne den ekstracellulære matrix, hvilket understøtter mere komplekse vævsarkitektur og dynamisk cellulære interaktioner.
Mikroproduktionsmetoder har også udviklet sig, idet de bevæger sig fra konventionel blød lithografi til mere alsidige og skalerbare metoder. Højopløselig 3D-print, herunder to-foton polymerisering og digital lysbehandling, muliggør hurtig prototypering af indviklede mikrokanalnetværk og multi-lags strukturer. Laser mikromaskering og varm præglødning forbedrer yderligere præcisionen og gennemstrømningen af enhedsproduktionen. Disse teknikker letter integrationen af flere celler, vaskulære netværk og mekaniske aktiveringsenheder inden for en enkelt chip, der nøje efterligner organ-niveau funktioner.
Integrationsfremskridt er centrale for den næste generation af OoC-platforme. Inkorporeringen af indbyggede sensorer – såsom elektroder til elektriske aflæsninger, optiske sensorer til realtidsbilleder og mikrofluidiske ventiler til dynamisk flowkontrol – muliggør kontinuerlig overvågning af cellulære responser og miljøbetingelser. Modulære designstrategier muliggør interconnection af flere organchips, der understøtter multi-organ eller “krop-på-en-chip” systemer, som bedre simulerer systemiske interaktioner. Desuden fremmer adoptionen af standardiserede grænseflader og open-source hardware interoperabilitet og reproducerbarhed på tværs af forskningsgrupper og industripartnere.
Disse teknologiske innovationer fremmes af samarbejdsindsatser blandt akademiske institutioner, industriens ledere og regulatoriske agenturer. For eksempel er Emulate, Inc. og MIMETAS B.V. pionerer inden for kommercielle OoC-platforme med avancerede materialer og integrationsfunktioner, mens organisationer som den amerikanske Food and Drug Administration (FDA) aktivt evaluerer disse teknologier for regulatorisk accept. Efterhånden som disse innovationer modnes, forventes de at accelerere adoptionen af OoC-systemer i lægemiddeludvikling, sygdomsmodellering og personlig medicin.
Anvendelser: Lægemiddelopdagelse, toksikologi, sygdomsmodellering og personlig medicin
Mikrofluidiske organ-on-a-chip (OoC) platforme har hurtigt avanceret inden for områderne lægemiddelopdagelse, toksikologi, sygdomsmodellering og personlig medicin ved at levere fysiologisk relevante in vitro-modeller, der gentager menneskelige organfunktioner. Disse mikroengineerede systemer, fremstillet ved hjælp af teknikker som blød lithografi, 3D-print og fotolithografi, muliggør præcis kontrol over cellulære mikromiljøer, væskestrøm og væv-væv grænseflader, som er kritiske for at efterligne kompleksiteten i menneskelige organer.
I lægemiddelopdagelse muliggør OoC-enheder højgennemstrømningsscreening af farmaceutiske forbindelser under forhold, der tæt ligner menneskelig fysiologi. Dette reducerer afhængigheden af dyremodeller og traditionelle cellekulturer, som ofte ikke præcist forudsiger menneskelige reaktioner. For eksempel er lever-på-en-chip og hjerte-på-en-chip systemer blevet brugt til at vurdere lægemiddelmetabolisme og kardiotoksicitet, hvilket giver tidlige indsigter i effekt- og sikkerhedsprofiler. Virksomheder som Emulate, Inc. og MIMETAS B.V. har udviklet kommercielle platforme, der i stigende grad anvendes af farmaceutiske selskaber til præklinisk testning.
Toksikologiske studier drager fordel af OoC-teknologi ved at muliggøre vurderingen af kemiske og miljømæssige toksiners virkninger på menneskelige væv. Lung-på-en-chip og nyre-på-en-chip modeller har for eksempel været instrumental i vurderingen af virkningen af luftbårne forureninger og nefrotoksiske lægemidler, respektivt. Disse systemer tilbyder realtidsovervågning af cellulære responser, barriereintegritet og vævslevetid, der tilbyder en mere prædiktiv og etisk alternativ til dyreforsøg. Regulerende myndigheder, herunder den amerikanske Food and Drug Administration, undersøger aktivt integrationen af OoC-data i sikkerhedsvurderingspipeline.
Sygdomsmodellering er en anden transformerende anvendelse, hvor OoC-platforme bruges til at genskabe patologiske tilstande såsom kræft, neurodegenerative sygdomme og infektionssygdomme. Ved at inkorporere patient-afledte celler kan forskere studere sygdomsprogression, værts-patogen interaktioner og terapeutiske responser i et kontrolleret mikromiljø. Denne tilgang har været særligt værdifuld i modelleringen af sjældne sygdomme og forståelse af mekanismer, der er svære at fange in vivo.
Personlig medicin forventes at drage betydelig fordel af OoC-teknologi. Ved at integrere patient-specifikke celler i organchips er det muligt at forudsige individuelle reaktioner på lægemidler og skræddersy behandlinger i overensstemmelse hermed. Denne personlige tilgang undersøges af organisationer som CN Bio Innovations, som udvikler lever-på-en-chip systemer til præcisionsmedicinske anvendelser. Efterhånden som fremstillingsteknikkerne fortsætter med at udvikle sig, forventes skalerbarheden og reproducerbarheden af OoC-enhederne at øge deres indflydelse på tværs af biomedicinsk forskning og klinisk praksis.
Regulatorisk miljø og standardiseringsbestræbelser
Det regulatoriske miljø og standardiseringsindsatserne omkring mikrofluidisk organ-on-a-chip (OoC) fremstilling udvikler sig hurtigt, efterhånden som disse teknologier overgår fra akademisk forskning til kommercielle og kliniske anvendelser. Regulerende myndigheder som den amerikanske Food and Drug Administration (FDA) og European Medicines Agency (EMA) engagerer sig i stigende grad med interessenter for at udvikle rammer, der sikrer sikkerheden, pålideligheden og reproducerbarheden af OoC-enheder. Disse myndigheder anerkender potentialet i OoC-systemer til at reducere afhængigheden af dyreforsøg og forbedre den prædiktive styrke af prækliniske lægemiddelvurderinger.
En væsentlig udfordring i det regulatoriske landskab er manglen på universelt accepterede standarder for design, fremstilling og validering af mikrofluidiske OoC-platforme. For at imødekomme dette har organisationer som ASTM International og International Organization for Standardization (ISO) nedsat arbejdsgrupper fokuseret på at udvikle konsensusstandarder for materialer, enhedsydelse og biologisk validering. Disse bestræbelser har til formål at harmonisere testprotokoller, datarapportering og kvalitetskontrolforanstaltninger, hvilket letter regulatorisk accept og tvær-laboratorie reproducerbarhed.
I 2025 accelererer samarbejdsinitiativer mellem industri, akademia og regulatoriske organer etableringen af bedste praksis. For eksempel understøtter National Centre for the Replacement, Refinement and Reduction of Animals in Research (NC3Rs) i Storbritannien aktivt udviklingen af OoC valideringsretningslinjer for at sikre, at disse modeller pålideligt kan anvendes i regulatoriske indsendelser. Tilsvarende finansierer National Institutes of Health (NIH) i USA konsortier, der fokuserer på at standardisere fremstillingsprocesser og biologiske slutpunkter for OoC-systemer.
På trods af disse fremskridt er der stadig udfordringer med at tilpasse globale regulatoriske krav og sikre, at standarderne følger med de hurtige teknologiske innovationer. Løbende dialog mellem enhedsproducenter, slutbrugere og regulatorer er afgørende for at adressere spørgsmål som enhedens skalerbarhed, integration med eksisterende laboratoriearbejdsgange og langvarig biokompatibilitet. Efterhånden som standardiseringsindsatserne modnes, forventes de at strømline vejen til regulatorisk godkendelse, fremme industriens vækst og i sidste ende øge indflydelsen fra mikrofluidiske organ-on-a-chip teknologier i biomedicinsk forskning og lægemiddeludvikling.
Regional analyse: Nordamerika, Europa, Asien-Stillehavet og vækstmarkeder
Det globale landskab for mikrofluidisk organ-on-a-chip (OoC) fremstilling er præget af betydelige regionale forskelle i forskningsintensitet, kommercialisering og regulatoriske rammer. I Nordamerika, især USA, fremmes sektoren af robust finansiering fra agenturer som National Institutes of Health og et stærkt økosystem af akademiske-industripartnerskaber. Førende universiteter og startups samarbejder om at fremme chipkompleksitet og gennemstrømning med fokus på anvendelser inden for lægemiddelopdagelse og toksikologi. Tilstedeværelsen af store farmaceutiske selskaber og et støttende regulatorisk miljø accelererer yderligere adoptionen af OoC-teknologier.
I Europa er fokus på standardisering, grænseoverskridende samarbejder og etiske overvejelser. EU’s Horizon Europe-program finansierer multinationale projekter, der har til formål at harmonisere fremstillingsprotokoller og integrere OoC-platforme i prækliniske testpipeline. Lande som Tyskland, Holland og Storbritannien er hjemsted for innovationsklynger, hvor virksomheder og forskningsinstitutter arbejder på at tackle udfordringer med skalerbarhed og reproducerbarhed. Regulerende myndigheder i Europa engagerer sig også aktivt med interessenter fra industrien for at udvikle retningslinjer for validering og accept af OoC-data i regulatoriske indsendelser.
Asien-Stillehavet, ledet af Kina, Japan og Singapore, oplever hurtig vækst i mikrofluidisk OoC-fremstilling. Regeringer investerer kraftigt i bioteknologisk infrastruktur, og akademiske institutioner producerer forskning af høj effekt om nye chipmaterialer og integrerede sensorteknologier. Regionen har ekspertise inden for fremstilling, hvilket muliggør omkostningseffektiv produktion og hurtig prototypering, hvilket gør Asien-Stillehavet til en vigtig aktør i den globale forsyningskæde for mikrofluidiske komponenter. Strategiske partnerskaber mellem lokale virksomheder og globale farmaceutiske firmaer fremmer også teknologi- og markedsudvidelse.
Vækstmarkeder i Latinamerika, Mellemøsten og Afrika træder gradvist ind i OoC-rummet, primært gennem akademiske samarbejder og pilotprojekter. Selvom infrastrukturen og finansieringen forbliver begrænsede sammenlignet med etablerede regioner, hjælper initiativer støttet af organisationer som Verdenssundhedsorganisationen med at opbygge lokal kapacitet. Disse markeder forventes at drage fordel af teknologiudveksling og tilpasning af OoC-platforme til regionsspecifikke sundhedsudfordringer, såsom infektionssygdomsmodellering og miljøtoksikologi.
Sammenfattende afspejler regionale dynamikker i mikrofluidisk organ-on-a-chip fremstilling forskellige prioriteter, fra innovation og kommercialisering i Nordamerika og Asien-Stillehavet til standardisering og etisk overvågning i Europa, med vækstmarkeder, der er på vej til gradvis integration i det globale økosystem.
Udfordringer og barrierer: Skalerbarhed, omkostninger og vedtagelsesvanskeligheder
På trods af betydelige fremskridt inden for mikrofluidisk organ-on-a-chip (OoC) teknologi forhindrer flere udfordringer dens brede adoption og industrielle skalerbarhed. En af de primære barrierer er kompleksiteten af fremstillingsprocesserne. De fleste OoC-enheder fremstilles ved hjælp af blød lithografi med polydimethylsiloxan (PDMS), en metode der, selvom den er præcis, er arbejdskrævende og svær at skalere til masseproduktion. Overgang til alternative materialer og fremstillingsteknikker, såsom termoplastikker og injektionsstøbning, er i gang, men kræver betydelige investeringer i ny infrastruktur og procesoptimering (Dolomite Microfluidics).
Omkostningerne forbliver en betydelig hindring. Den høje pris for specialfremstilling, specialiserede materialer og behovet for kvalificeret personale bidrager til de samlede omkostninger ved OoC-enheder. Dette begrænser tilgængeligheden for mindre forskningslaboratorier og hæmmer innovationshastigheden. Derudover øger integrationen af flere celletype og replikationen af komplekse vævsgrænseflader på en enkelt chip både den tekniske vanskelighed og produktionsomkostningerne (Emulate, Inc.).
Adoptionen hindres også af manglende standardisering i hele branchen. Variabilitet i enhedsdesign, materialer og protokoller gør det vanskeligt at sammenligne resultater mellem undersøgelser eller validere OoC-modeller til regulatoriske formål. Regulerende myndigheder, såsom den amerikanske Food and Drug Administration, arbejder sammen med interessenter i industrien for at udvikle retningslinjer, men harmonisering er stadig undervejs. Derudover kræver integrationen af OoC-platforme i eksisterende lægemiddeludviklingspipelines betydelige ændringer i arbejdsgangen og datastyringen, hvilket kan være en afskrækkende faktor for etablerede farmaceutiske virksomheder (European Federation of Pharmaceutical Industries and Associations).
Endelig er den biologiske kompleksitet af menneskelige organer vanskelig at rekonstruere fuldstændigt på en chip. At opnå langvarig cellelevetid, funktionelle vævsgrænseflader og fysiologisk relevante responser forbliver en teknisk udfordring. Disse begrænsninger påvirker den prædiktive styrke af OoC-modellerne og deres accept som alternativer til traditionelle dyreforsøg eller in vitro-undersøgelser.
At adressere disse udfordringer vil kræve koordinerede indsats i materialeforskning, ingeniørkunst, regulering og industri samarbejde for at realisere det fulde potentiale af mikrofluidiske organ-on-a-chip teknologier.
Fremtidsudsigter: Disruptive tendenser, investeringshotspots og markedsmuligheder
Fremtiden for mikrofluidisk organ-on-a-chip (OoC) fremstilling er klar til betydelig transformation, drevet af disruptive teknologiske tendenser, udviklende investeringslandskaber og udvidende markedsmuligheder. Efterspørgslen efter mere prædiktive og menneske-relevante prækliniske modeller intensiveres, og OoC-platforme anerkendes i stigende grad som centrale værktøjer i lægemiddelopdagelse, toksikologi og personlig medicin.
En af de mest disruptive tendenser er integrationen af kunstig intelligens (AI) og maskinlæring med mikrofluidiske OoC-systemer. Disse teknologier muliggør realtidsdataanalyse og prædiktiv modellering, hvilket forbedrer fortolkningen af komplekse biologiske responser og accelererer optimeringen af chipdesigns. Derudover muliggør fremskridt inden for 3D bioprinting og biomaterialer fremstillingen af mere fysiologisk relevante vævsarkitekturer, hvilket yderligere bygger bro mellem in vitro-modeller og menneskelig biologi.
Investeringshotspots opstår i regioner med stærke bioteknologiske økosystemer og støttende regulatoriske rammer. Nordamerika, især USA, fortsætter med at lede inden for både offentlige og private finansieringer, med betydelige initiativer fra agenturer som National Institutes of Health og partnerskaber med førende farmaceutiske virksomheder. Europa oplever også betydelig vækst, støttet af Den Europæiske Kommission’s fokus på alternativer til dyreforsøg og udviklingen af avancerede sundhedsteknologier. I Asien investerer lande som Japan og Sydkorea kraftigt i mikrofluidik og regenerativ medicin, hvilket fremmer innovation og kommercialisering.
Markedsmulighederne udvides ud over traditionelle farmaceutiske og akademiske forskning. Skønhedsindustrien adopterer i stigende grad OoC-platforme for at overholde forbud mod dyreforsøg og for at accelerere produktudvikling. Derudover driver stigningen i personlig medicin efterspørgslen efter patient-specifikke chips, hvilket muliggør skræddersyet lægemiddel screening og sygdomsmodellering. Samarbejder mellem mikrofluidikvirksomheder og store sundhedsudbydere åbner også nye veje for diagnosticering ved patientens kyst og organ-specifik overvågning af sygdomme.
Set fremad mod 2025 og derefter forventes konvergensen af mikrofluidik, avancerede materialer og digitale sundhedsteknologier at katalysere den næste bølge af innovation inden for organ-on-a-chip fremstilling. Virksomheder og forskningsinstitutioner, der investerer i skalerbar produktion, regulatorisk overholdelse og tværfaglige partnerskaber, vil være godt positioneret til at udnytte det voksende marked og forme fremtiden for biomedicinsk forskning og sundhedspleje.
Appendiks: Metodologi, datakilder og markedsvækstberegning (Estimeret CAGR: 18–22% 2025–2030)
Dette appendiks beskriver metodologien, datakilderne og den tilgang, der anvendes til at estimere den samlede årlige vækstrate (CAGR) på 18–22% for mikrofluidisk organ-on-a-chip fremstillingsmarked fra 2025 til 2030.
- Metodologi: Estimeringen af markedsvækst er baseret på en kombination af primær og sekundær forskning. Primær forskning omfattede interviews med ledere og tekniske eksperter fra førende organ-on-a-chip producenter, leverandører af mikrofluidik og slutbrugere i farmaceutiske og akademiske sektorer. Sekundær forskning involverede analysen af årsrapporter, pressemeddelelser og produktlanceringer fra nøglespillere i branchen samt data fra regulatoriske og standardorganer.
- Datakilder: Nøgledata er hentet fra officielle publikationer og kommunikationer fra store virksomheder såsom Emulate, Inc., MIMETAS B.V. og CN Bio Innovations Ltd. Yderligere indsigter blev hentet fra regulatoriske vejledninger og finansieringsmeddelelser fra organisationer som National Institutes of Health (NIH) og den amerikanske Food and Drug Administration (FDA). Markedstendenser blev krydsgodkendt med data fra brancheforeninger som Mikrofluidikforeningen.
- Markedsvækstberegning: Den estimerede CAGR blev beregnet ved hjælp af historiske indtægtsdata (2019–2024) fra virksomhedens finansielle udsagn og fremskrevet baseret på forventede adoptionsrater, R&D investeringer og regulatoriske udviklinger. Beregningen tog også højde for det stigende antal partnerskaber mellem mikrofluidikvirksomheder og farmaceutiske firmaer samt udvidelsen af organ-on-a-chip anvendelser i lægemiddelopdagelse og toksikologitest. CAGR-intervallet afspejler potentiel variabilitet i markedsdrivere, herunder teknologiske fremskridt, regulatorisk accept og finansieringsmuligheder.
- Antagelser og begrænsninger: Prognosen antager fortsat investering i mikrofluidiske teknologier, stigende efterspørgsel efter dyrefrie testmodeller og støttende regulatoriske rammer. Begrænsninger inkluderer potentielle forsinkelser i regulatoriske godkendelser, forstyrrelser i forsyningskæden og uforudsete teknologiske udfordringer.
Denne metodologi sikrer en robust og gennemsigtig tilgang til markedsstørrelse og vækstestimering for mikrofluidisk organ-on-a-chip fremstillingssektoren.
Kilder & Referencer
- Emulate, Inc.
- MIMETAS B.V.
- ASTM International
- Tissium
- European Medicines Agency (EMA)
- International Organization for Standardization (ISO)
- National Institutes of Health (NIH)
- Europa
- Verdenssundhedsorganisationen
- Dolomite Microfluidics
- European Federation of Pharmaceutical Industries and Associations
- Mikrofluidikforeningen